1 材料与方法
1.1 数据来源
1.2 家族成员鉴定
1.3 基因结构与蛋白质保守基序分析
1.4 系统发育进化分析
1.5 蛋白的理化性质分析
1.6 磷酸位点预测
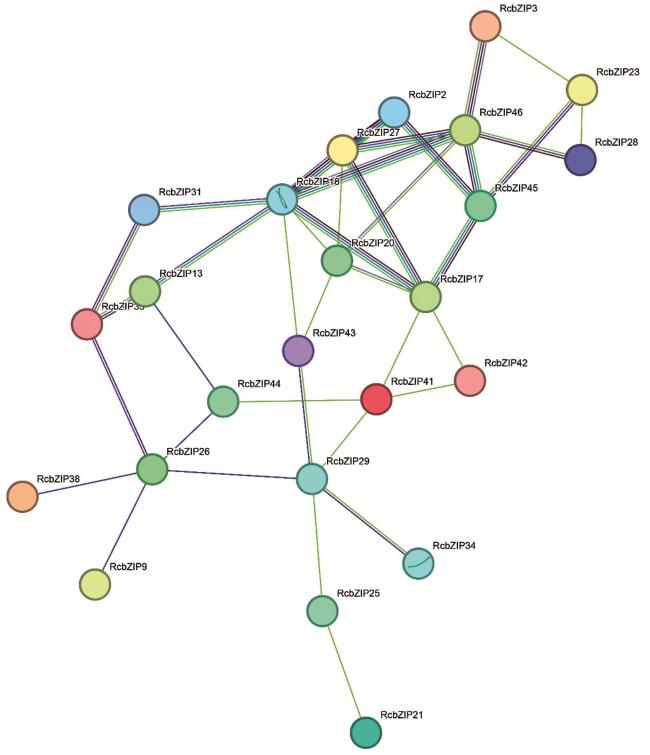
1.7 蛋白互作网络分析
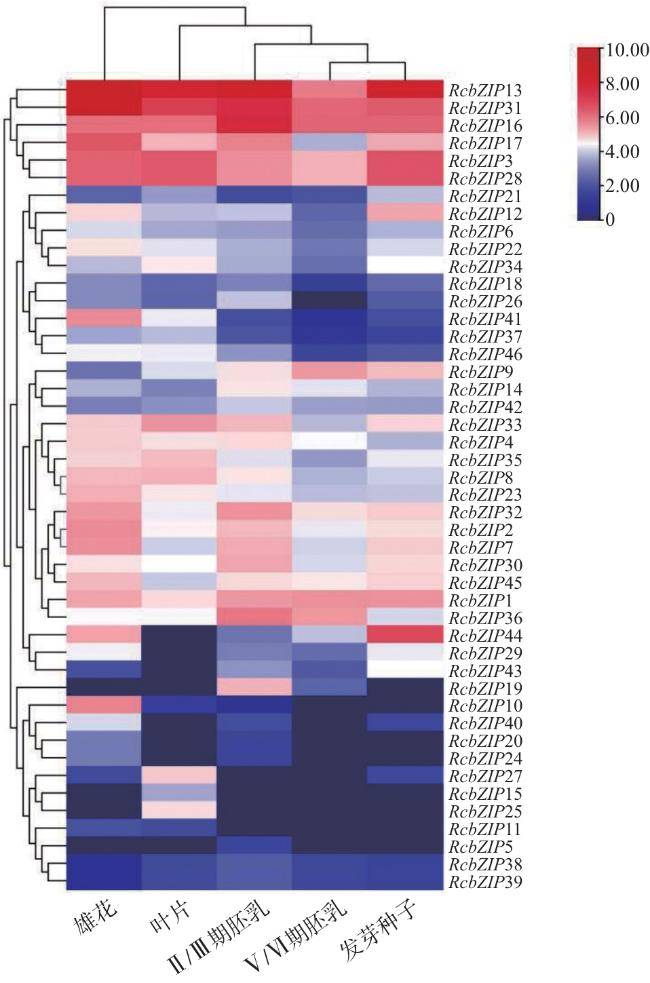
1.8 表达模式分析
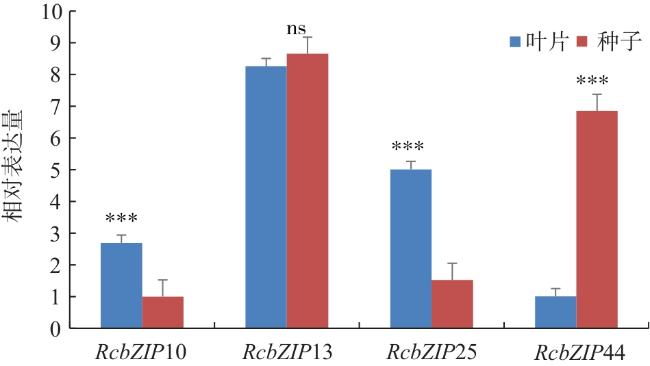
1.9 荧光定量分析
2 结果与分析
2.1 家族成员鉴定
表1 蓖麻bZIP基因家族基础信息 |
| 基因名称 | 基因ID | 染色体定位 | 起始位置 | 终止位置 | 基因长度/bp |
|---|---|---|---|---|---|
| RcbZIP1 | Rc01T000398 | Chr1 | 2607841 | 2612902 | 5 061 |
| RcbZIP2 | Rc01T000839 | Chr1 | 5893950 | 5902544 | 8 594 |
| RcbZIP3 | Rc01T001217 | Chr1 | 8565590 | 8566255 | 665 |
| RcbZIP4 | Rc01T002251 | Chr1 | 30245570 | 30253388 | 7 818 |
| RcbZIP5 | Rc02T003294 | Chr2 | 17749819 | 17755449 | 5 630 |
| RcbZIP6 | Rc02T003449 | Chr2 | 24834808 | 24838157 | 3 349 |
| RcbZIP7 | Rc02T003897 | Chr2 | 29860176 | 29865949 | 5 773 |
| RcbZIP8 | Rc02T003919 | Chr2 | 30084042 | 30088552 | 4 510 |
| RcbZIP9 | Rc02T004176 | Chr2 | 32096294 | 32102356 | 6 062 |
| RcbZIP10 | Rc02T004177 | Chr2 | 32108030 | 32109631 | 1 601 |
| RcbZIP11 | Rc02T004453 | Chr2 | 34291174 | 34291650 | 476 |
| RcbZIP12 | Rc02T004588 | Chr2 | 35220180 | 35223880 | 3 700 |
| RcbZIP13 | Rc02T004777 | Chr2 | 36552346 | 36553192 | 846 |
| RcbZIP14 | Rc02T004830 | Chr2 | 36899294 | 36903292 | 3 998 |
| RcbZIP15 | Rc02T004911 | Chr2 | 37429621 | 37431403 | 1 782 |
| RcbZIP16 | Rc02T005044 | Chr2 | 38281295 | 38292857 | 11 562 |
| RcbZIP17 | Rc03T005091 | Chr3 | 163929 | 167200 | 3 271 |
| RcbZIP18 | Rc03T005285 | Chr3 | 1444360 | 1447723 | 3 363 |
| RcbZIP19 | Rc04T008282 | Chr4 | 8219465 | 8220037 | 572 |
| RcbZIP20 | Rc04T008328 | Chr4 | 8495515 | 8496117 | 602 |
| RcbZIP21 | Rc04T008407 | Chr4 | 9245792 | 9251707 | 5 915 |
| RcbZIP22 | Rc04T009000 | Chr4 | 21320232 | 21324080 | 3 848 |
| RcbZIP23 | Rc05T009921 | Chr5 | 4420854 | 4428233 | 7 379 |
| RcbZIP24 | Rc05T011696 | Chr5 | 21618539 | 21619126 | 587 |
| RcbZIP25 | Rc05T012599 | Chr5 | 30441694 | 30443770 | 2 076 |
| RcbZIP26 | Rc05T012714 | Chr5 | 31518730 | 31519435 | 705 |
| RcbZIP27 | Rc06T012799 | Chr6 | 56132 | 62180 | 6 048 |
| RcbZIP28 | Rc06T012916 | Chr6 | 846786 | 848109 | 1 323 |
| RcbZIP29 | Rc07T014987 | Chr7 | 361606 | 369644 | 8 038 |
| RcbZIP30 | Rc07T015466 | Chr7 | 5259928 | 5265249 | 5 321 |
| RcbZIP31 | Rc07T017223 | Chr7 | 28399105 | 28399584 | 479 |
| RcbZIP32 | Rc07T017285 | Chr7 | 28855716 | 28859928 | 4 212 |
| RcbZIP33 | Rc07T017304 | Chr7 | 28989825 | 28997958 | 8 133 |
| RcbZIP34 | Rc08T017460 | Chr8 | 417680 | 425859 | 8 179 |
| RcbZIP35 | Rc08T017991 | Chr8 | 4944615 | 4951605 | 6 990 |
| RcbZIP36 | Rc08T018588 | Chr8 | 18455992 | 18466572 | 10 580 |
| RcbZIP37 | Rc08T019517 | Chr8 | 29401615 | 29409512 | 7 897 |
| RcbZIP38 | Rc09T021235 | Chr9 | 21560119 | 21564179 | 4 060 |
| RcbZIP39 | Rc09T021236 | Chr9 | 21591593 | 21598622 | 7 029 |
| RcbZIP40 | Rc09T021550 | Chr9 | 24686426 | 24705610 | 19 184 |
| RcbZIP41 | Rc09T021863 | Chr9 | 27474932 | 27478571 | 3 639 |
| RcbZIP42 | Rc10T022321 | Chr10 | 2135605 | 2140072 | 4 467 |
| RcbZIP43 | Rc10T022347 | Chr10 | 2339351 | 2343050 | 3 699 |
| RcbZIP44 | Rc10T022643 | Chr10 | 4893306 | 4900250 | 6 944 |
| RcbZIP45 | Rc10T023016 | Chr10 | 10022264 | 10026359 | 4 095 |
| RcbZIP46 | Rc10T024171 | Chr10 | 24032790 | 24036213 | 3 423 |
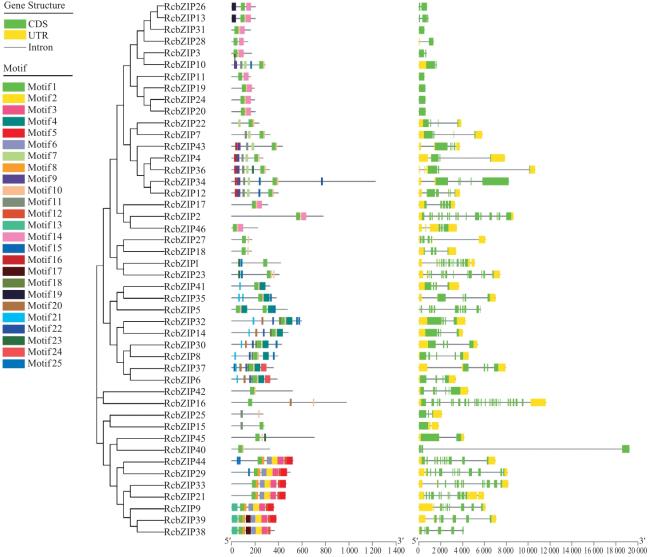
2.2 蓖麻bZIP基因结构与蛋白质保守基序
表2 蓖麻bZIP基因家族内含子、外显子数量 |
| 分组 | 基因名称 | 外显子数/个 | 内含子数/个 |
|---|---|---|---|
| Ⅰ组 | RcbZIP26 | 2 | 1 |
| RcbZIP13 | 2 | 1 | |
| RcbZIP31 | 1 | 0 | |
| RcbZIP28 | 2 | 1 | |
| RcbZIP3 | 2 | 1 | |
| RcbZIP10 | 2 | 1 | |
| Ⅱ组 | RcbZIP11 | 1 | 0 |
| RcbZIP19 | 1 | 0 | |
| RcbZIP24 | 1 | 0 | |
| RcbZIP20 | 1 | 0 | |
| Ⅲ组 | RcbZIP22 | 4 | 3 |
| RcbZIP7 | 4 | 3 | |
| Ⅳ组 | RcbZIP43 | 6 | 5 |
| RcbZIP4 | 4 | 3 | |
| RcbZIP36 | 5 | 4 | |
| RcbZIP34 | 6 | 5 | |
| RcbZIP12 | 6 | 5 | |
| Ⅴ组 | RcbZIP17 | 5 | 4 |
| RcbZIP2 | 16 | 15 | |
| RcbZIP46 | 5 | 4 | |
| Ⅵ组 | RcbZIP27 | 5 | 4 |
| RcbZIP18 | 4 | 3 | |
| RcbZIP1 | 15 | 14 | |
| RcbZIP23 | 13 | 12 | |
| Ⅶ组 | RcbZIP41 | 4 | 3 |
| RcbZIP35 | 5 | 4 | |
| RcbZIP5 | 11 | 10 | |
| RcbZIP32 | 4 | 3 | |
| RcbZIP14 | 4 | 3 | |
| RcbZIP30 | 2 | 1 | |
| RcbZIP8 | 5 | 4 | |
| RcbZIP37 | 5 | 4 | |
| RcbZIP6 | 4 | 3 | |
| Ⅷ组 | RcbZIP42 | 6 | 5 |
| RcbZIP16 | 26 | 25 | |
| Ⅸ组 | RcbZIP25 | 3 | 2 |
| RcbZIP15 | 2 | 1 | |
| Ⅹ组 | RcbZIP45 | 2 | 1 |
| RcbZIP40 | 3 | 2 | |
| Ⅺ组 | RcbZIP44 | 11 | 10 |
| RcbZIP29 | 13 | 12 | |
| RcbZIP33 | 12 | 11 | |
| RcbZIP21 | 12 | 11 | |
| RcbZIP9 | 10 | 9 | |
| RcbZIP39 | 7 | 6 | |
| RcbZIP38 | 6 | 5 |
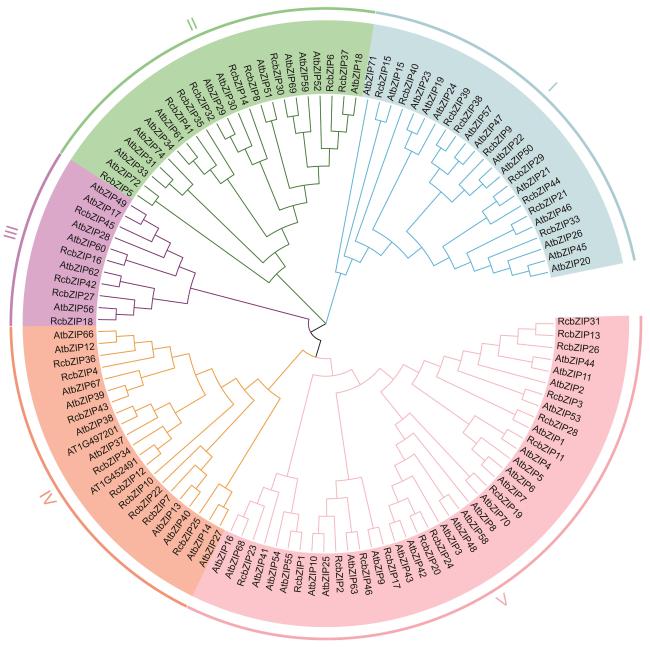
2.3 系统发育进化树
2.4 蛋白质理化性质
表3 蓖麻bZIP蛋白理化性质信息 |
| 蛋白名称 | 氨基酸 数/个 | 分子 量/D | 等电点 | 不稳定系数 | 疏水系数 | 亚细胞 定位 |
|---|---|---|---|---|---|---|
| RcbZIP1 | 415 | 44 566.66 | 7.83 | 54.45 | -0.747 | 细胞核 |
| RcbZIP2 | 778 | 84 425.63 | 7.18 | 51.62 | -0.453 | 细胞核 |
| RcbZIP3 | 170 | 19 301.77 | 5.91 | 59.73 | -0.604 | 细胞核 |
| RcbZIP4 | 267 | 30 247.15 | 8.98 | 61.51 | -0.741 | 细胞核 |
| RcbZIP5 | 474 | 55 104.72 | 9.15 | 53.44 | -0.770 | 细胞核 |
| RcbZIP6 | 386 | 41 770.19 | 6.28 | 53.31 | -0.859 | 细胞核 |
| RcbZIP7 | 324 | 35 726.13 | 7.80 | 63.03 | -0.738 | 细胞核 |
| RcbZIP8 | 391 | 42 439.49 | 7.28 | 40.23 | -0.560 | 细胞核 |
| RcbZIP9 | 361 | 40 689.76 | 6.57 | 48.55 | -0.476 | 细胞核 |
| RcbZIP10 | 285 | 32 293.18 | 5.38 | 55.96 | -0.665 | 细胞核 |
| RcbZIP11 | 158 | 18 310.67 | 8.57 | 63.23 | -0.568 | 细胞核 |
| RcbZIP12 | 395 | 43 454.42 | 9.74 | 48.14 | -0.819 | 细胞核 |
| RcbZIP13 | 201 | 23 028.24 | 9.00 | 71.46 | -0.265 | 细胞核 |
| RcbZIP14 | 481 | 52 558.70 | 6.54 | 61.97 | -0.640 | 细胞核 |
| RcbZIP15 | 277 | 31 272.28 | 10.06 | 76.36 | -0.640 | 细胞核 |
| RcbZIP16 | 975 | 107 255.96 | 6.19 | 44.5 | -0.289 | 叶绿体 |
| RcbZIP17 | 308 | 34 391.13 | 5.13 | 61.19 | -0.788 | 细胞核 |
| RcbZIP18 | 169 | 18 610.46 | 9.83 | 66.7 | -1.200 | 细胞核 |
| RcbZIP19 | 190 | 21 589.17 | 9.26 | 65.75 | -0.793 | 细胞核 |
| RcbZIP20 | 200 | 22 929.48 | 5.89 | 67.1 | -0.789 | 细胞核 |
| RcbZIP21 | 459 | 50 795.69 | 5.96 | 45.18 | -0.509 | 细胞核 |
| RcbZIP22 | 231 | 26 457.11 | 5.53 | 57.39 | -1.119 | 细胞核 |
| RcbZIP23 | 405 | 43 100.31 | 6.11 | 54.24 | -0.882 | 细胞核 |
| RcbZIP24 | 195 | 22 835.22 | 5.58 | 73.51 | -0.937 | 细胞核 |
| RcbZIP25 | 267 | 29 428.45 | 8.17 | 54.96 | -0.631 | 细胞膜、细胞核 |
| RcbZIP26 | 201 | 23 272.47 | 8.89 | 66.45 | -0.391 | 细胞核 |
| RcbZIP27 | 172 | 19 529.94 | 9.83 | 57.88 | -1.018 | 细胞核 |
| RcbZIP28 | 136 | 15 781.28 | 9.28 | 59.81 | -0.746 | 细胞核 |
| RcbZIP29 | 498 | 55 044.86 | 6.94 | 54.01 | -0.547 | 细胞核 |
| RcbZIP30 | 425 | 46 528.41 | 6.09 | 59.27 | -0.825 | 细胞核 |
| RcbZIP31 | 159 | 17 660.67 | 6.29 | 56.43 | -0.542 | 细胞核 |
| RcbZIP32 | 595 | 65 026.57 | 6.23 | 64.55 | -0.881 | 细胞核 |
| RcbZIP33 | 463 | 51 139.05 | 5.64 | 56.05 | -0.539 | 细胞核 |
| RcbZIP34 | 1 223 | 135 988.36 | 8.18 | 35.53 | -0.220 | 细胞核 |
| RcbZIP35 | 380 | 42 702.17 | 8.28 | 73.95 | -0.978 | 细胞核 |
| RcbZIP36 | 321 | 36 103.80 | 8.79 | 48.44 | -0.846 | 细胞核 |
| RcbZIP37 | 355 | 39 712.36 | 6.01 | 58.83 | -0.787 | 细胞核 |
| RcbZIP38 | 363 | 40 739.67 | 5.78 | 49.26 | -0.203 | 细胞核 |
| RcbZIP39 | 382 | 43 188.59 | 8.43 | 51.01 | -0.278 | 细胞核 |
| RcbZIP40 | 320 | 36 163.74 | 8.75 | 46.44 | -0.645 | 细胞核 |
| RcbZIP41 | 325 | 36 319.17 | 6.60 | 56.64 | -0.830 | 细胞核 |
| RcbZIP42 | 515 | 55 889.82 | 8.53 | 61.08 | -0.643 | 细胞核 |
| RcbZIP43 | 433 | 47 274.50 | 9.18 | 52.88 | -0.749 | 细胞核 |
| RcbZIP44 | 521 | 58 431.56 | 6.70 | 60.59 | -0.652 | 细胞核 |
| RcbZIP45 | 702 | 76 224.99 | 6.73 | 38.86 | -0.591 | 细胞核 |
| RcbZIP46 | 220 | 24 567.66 | 7.88 | 56.00 | -0.559 | 细胞核 |
2.5 蛋白磷酸化位点预测
表4 蓖麻bZIP蛋白磷酸位点预测结果 |
| 蛋白名称 | 丝氨酸(Ser) | 苏氨酸(Thr) | 酪氨酸(Tyr) | 位点数/个 |
|---|---|---|---|---|
| RcbZIP1 | 42 | 13 | 5 | 60 |
| RcbZIP2 | 49 | 26 | 2 | 77 |
| RcbZIP3 | 12 | 2 | 2 | 16 |
| RcbZIP4 | 23 | 10 | 1 | 34 |
| RcbZIP5 | 31 | 5 | 7 | 43 |
| RcbZIP6 | 28 | 11 | 2 | 41 |
| RcbZIP7 | 28 | 11 | 2 | 41 |
| RcbZIP8 | 31 | 12 | 2 | 45 |
| RcbZIP9 | 24 | 12 | 6 | 42 |
| RcbZIP10 | 33 | 5 | 3 | 41 |
| RcbZIP11 | 19 | 4 | 0 | 23 |
| RcbZIP12 | 20 | 14 | 4 | 38 |
| RcbZIP13 | 24 | 4 | 1 | 29 |
| RcbZIP14 | 48 | 11 | 2 | 61 |
| RcbZIP15 | 39 | 10 | 4 | 53 |
| RcbZIP16 | 54 | 27 | 10 | 91 |
| RcbZIP17 | 28 | 9 | 2 | 39 |
| RcbZIP18 | 24 | 5 | 1 | 30 |
| RcbZIP19 | 22 | 2 | 1 | 25 |
| RcbZIP20 | 17 | 4 | 0 | 21 |
| RcbZIP21 | 26 | 17 | 4 | 47 |
| RcbZIP22 | 16 | 7 | 6 | 29 |
| RcbZIP23 | 37 | 14 | 4 | 55 |
| RcbZIP24 | 17 | 6 | 1 | 24 |
| RcbZIP25 | 37 | 18 | 5 | 60 |
| RcbZIP26 | 24 | 4 | 1 | 29 |
| RcbZIP27 | 14 | 4 | 2 | 20 |
| RcbZIP28 | 11 | 0 | 0 | 11 |
| RcbZIP29 | 32 | 18 | 3 | 53 |
| RcbZIP30 | 35 | 12 | 1 | 48 |
| RcbZIP31 | 12 | 5 | 2 | 19 |
| RcbZIP32 | 75 | 18 | 1 | 94 |
| RcbZIP33 | 41 | 13 | 2 | 56 |
| RcbZIP34 | 54 | 26 | 9 | 89 |
| RcbZIP35 | 36 | 5 | 7 | 48 |
| RcbZIP36 | 23 | 11 | 3 | 37 |
| RcbZIP37 | 29 | 9 | 1 | 39 |
| RcbZIP38 | 19 | 10 | 3 | 32 |
| RcbZIP39 | 16 | 10 | 3 | 29 |
| RcbZIP40 | 22 | 7 | 6 | 35 |
| RcbZIP41 | 26 | 9 | 1 | 36 |
| RcbZIP42 | 50 | 13 | 1 | 64 |
| RcbZIP43 | 34 | 16 | 3 | 53 |
| RcbZIP44 | 35 | 17 | 1 | 53 |
| RcbZIP45 | 64 | 14 | 6 | 84 |
| RcbZIP46 | 17 | 13 | 1 | 31 |