1 材料与方法
1.1 试验材料
1.2 试验方法
1.2.1 外植体消毒
1.2.2 诱导培养
1.2.3 增殖培养
1.2.4 生根培养
1.3 数据处理
2 结果与分析
2.1 不同消毒方法对初代培养效果的影响
表1 不同消毒方法对外植体消毒情况的影响 |
| 处理 | 75%乙醇消 毒时间/s | 0.5%苯扎溴铵 消毒时间/min | 接种30 d后 | ||||
|---|---|---|---|---|---|---|---|
| 褐化率/% | 真菌污染率/% | 细菌污染率/% | 存活率/% | 生长状况 | |||
| 10 20 30 | 10 15 20 | 1.5 0.5 7.0 | 5.5 1.0 2.0 | 2.0 2.5 0.5 | 91.0 96.0 90.5 | 状态佳 状态佳,接种7 d有芽 状态佳 | |
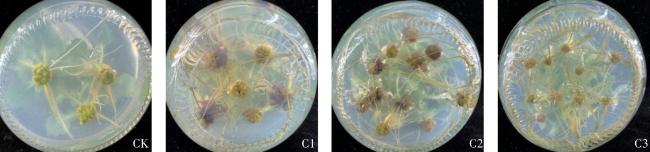
2.2 不同激素配比对组培苗芽诱导的影响
表2 不同激素配比对组培苗芽诱导的影响 |
| 培养基 | 6-BA/(mg/L) | NAA/(mg/L) | 有芽数/个 | 芽诱导率/% | 褐化数 | 褐化率/% |
|---|---|---|---|---|---|---|
| CK | 0 | 0 | 4.00±2.16 d | 10.00±5.40 d | 4.67±2.05 b | 11.67±5.14 b |
| A1 | 0.5 | 0.1 | 19.67±2.87 b | 49.17±7.17 b | 2.00±0.82 c | 5.00±2.04 c |
| A2 | 1.0 | 0.1 | 12.33±2.05 c | 30.83±5.14 c | 13.33±1.25 a | 33.33±3.12 a |
| A3 | 2.0 | 0.1 | 8.00±2.94 c | 20.00±7.36 c | 12.33±1.25 a | 30.83±3.12 a |
| A4 | 0.5 | 0.5 | 5.00±1.63 d | 12.50±4.08 d | 8.00±3.74 b | 20.00±9.35 b |
| A5 | 1.0 | 0.5 | 31.33±2.87 a | 78.33±7.17 a | 2.67±1.70 c | 6.67±4.25 c |
| A6 | 2.0 | 0.5 | 17.33±2.05 b | 43.33±5.14 b | 3.33±1.25 c | 8.33±3.12 c |
| A7 | 0.5 | 1.0 | 10.33±2.87 c | 25.83±7.17 c | 12.67±1.70 a | 31.67±4.25 a |
| A8 | 1.0 | 1.0 | 19.00±2.16 b | 47.50±5.40 b | 2.33±2.05 c | 5.83±5.14 c |
| A9 | 2.0 | 1.0 | 12.67±2.05 c | 31.67±5.14 c | 6.67±2.49 b | 16.67±6.24 b |
|