1 材料与方法
1.1 试验材料
1.2 试验试剂与仪器
1.3 实验方法
1.3.1 LMS的提取
1.3.2 细胞培养及LMS溶液配制
1.3.3 细胞增殖检测
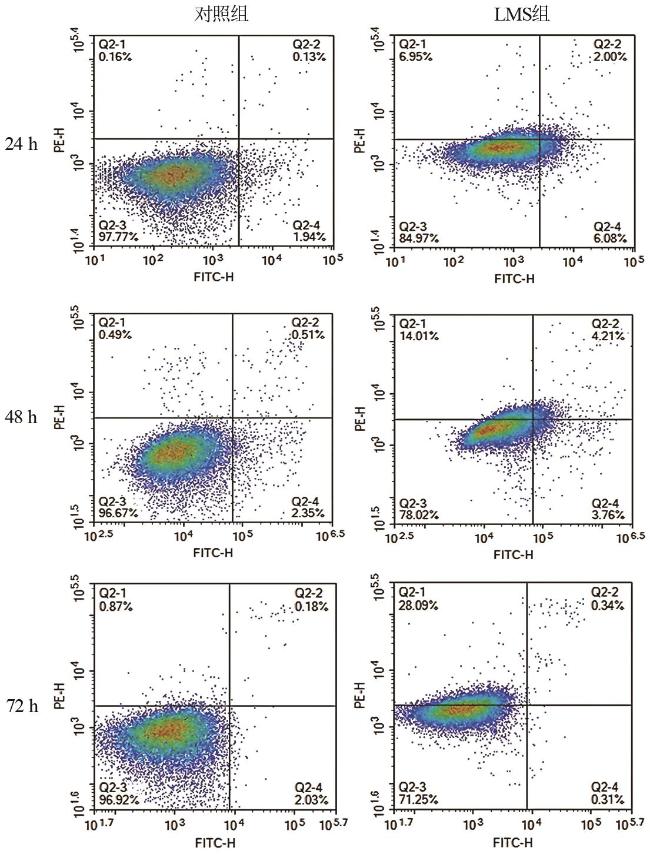
1.3.4 细胞凋亡率检测
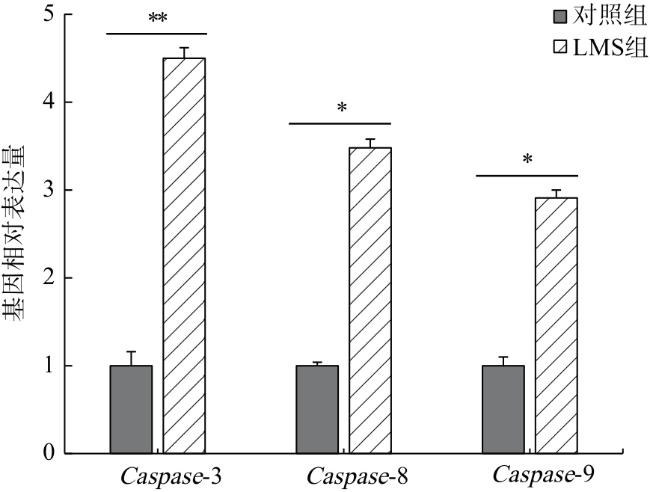
1.3.5 基因表达量检测
表1 引物序列 |
| 基因名称 | NCBI编号 | 引物序列(5'-3') | 大小/bp |
|---|---|---|---|
| | NM_032991.2 | F:GGTTCATCCAGTCGCTTTG R:ATTCTGTTGCCACCTTTCG | 99 |
| | NM_001228.4 | F:TTCCTGAGCCTGGACTACATT R:GAAGTTCCCTTTCCATCTCCT | 202 |
| | NM_001229.4 | F:ACTAACAGGCAAGCAGCAAA R:CCAAATCCTCCAGAACCAAT | 140 |
| β-actin | NM_001101.3 | F:CTGGGACGACATGGAGAAA R:GCACAGCCTGGATAGCAAC | 182 |
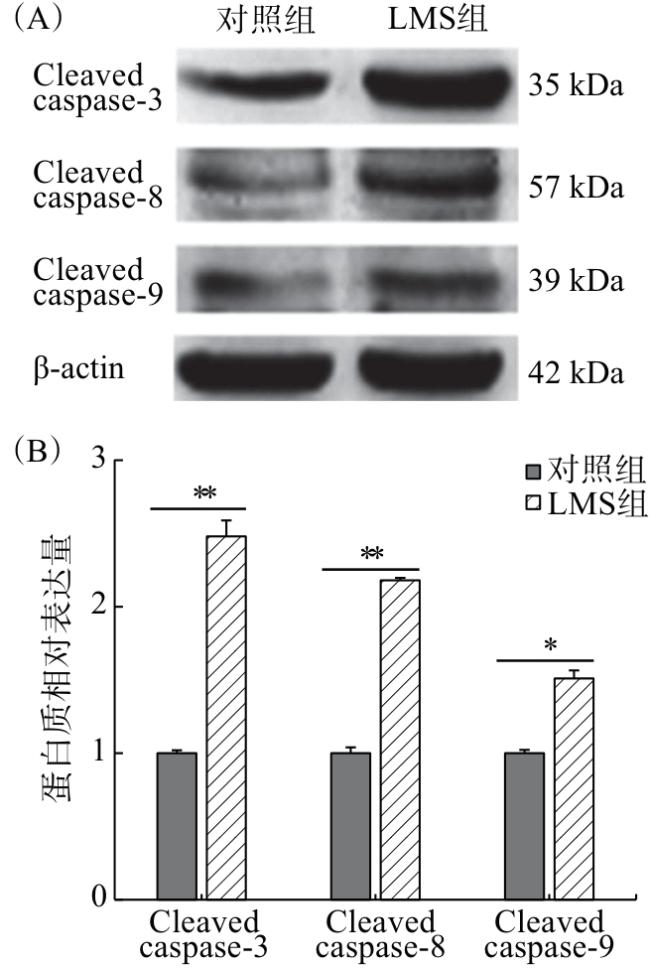
1.3.6 蛋白表达量检测
1.4 数据处理
2 结果与分析
2.1 LMS的提取得率
2.2 LMS对Y79细胞增殖的影响
表2 不同浓度LMS和处理时间对Y79细胞增殖的影响 (%) |
| LMS浓 度/(μg/mL) | 细胞存活率 | ||
|---|---|---|---|
| 24 h | 48 h | 72 h | |
| 0 | 94.34±0.67 | 93.70±0.84 | 94.07±1.51 |
| 100 | 93.37±1.22 | 88.33±2.19* | 41.08±3.24** |
| 200 | 89.13±2.55 | 70.26±3.56* | 30.85±2.37** |
| 400 | 78.27±3.38* | 54.05±2.97** | 23.95±2.84** |
| 800 | 31.93±3.04** | 18.50±0.71** | 12.30±1.35** |
|