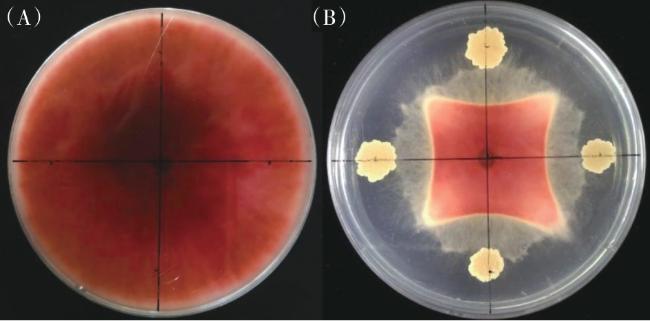
生物防治法作为小麦赤霉病化学防治手段的有益补充,受到越来越多关注。研究人员从不同生境中分离得到对禾谷镰刀菌具有拮抗作用的菌株,包括枯草芽孢杆菌、解淀粉芽孢杆菌、奇异变形杆菌和微白黄链霉菌等
[4,11]。贝莱斯芽孢杆菌是一种嗜温好氧细菌,在自然界中,尤其是土壤中广泛存在,因其抗逆性强、繁殖速度快、安全性高且对人畜无害等特点,适宜作生物防治菌种
[17]。王文肖等
[10]研究了贝莱斯芽孢杆菌EA19与多菌灵复配对小麦赤霉病的防效,结果表明,该菌株冻干粉与多菌灵联合施用,可使多菌灵在减量30%的同时,防效不受影响,具有良好的协同防治效果。曹荣耀等
[18]研究发现,贝莱斯芽孢杆菌能够抑制禾谷镰刀菌的生长,且该菌的培养上清液对禾谷镰刀菌具有较好的拮抗效果,但加热处理后拮抗性能显著降低。本研究结果表明,
B. velezensis SX1302能抑制禾谷镰刀菌的生长和小麦赤霉病的发生,并且抑制禾谷镰刀菌生长的活性物质具有热稳定性,121 ℃加热处理并不能降低其活性,可能是一种耐热的酶或者其他活性分子。贝莱斯芽孢杆菌已被应用于抑制病原真菌或细菌生长,但起拮抗作用的相关化合物暂不清楚。Gao等
[19]研究表明,贝莱斯芽孢杆菌对病原菌杀鲑气单胞菌具有较强的抑制作用,且抑菌相关物质具有耐热性。王冲等
[20]研究表明,贝莱斯芽孢杆菌Vel-HNGD-F2能够产生多种脂肽类物质,这些物质对禾谷镰刀菌具有较好的防治作用,且具有良好的耐热性,对紫外照射不敏感。本研究中,121 ℃加热处理无细胞上清液并不能降低其抑菌活性,说明菌株
B.velezensis SX1302产生的抑菌活性物质可能并不止一种,并且起主要抑菌作用的活性物质具有良好的耐热性。