在食品供应链等生态系统中,细菌生物被膜形成引发的抗生素耐药性增强问题已成为日益严峻的人类健康威胁
[1]。生物被膜是微生物通过自身分泌的胞外聚合物形成并附着于介质表面的微生物群落
[2]。细菌形成生物被膜后,生理活性会发生改变,其抗生素耐药性可提升10~1 000倍,给食品安全与医疗卫生领域带来严重隐患
[3-4]。乳酸菌无菌发酵上清液(Cell-free fermentation supernatant,CFS)对细菌生物被膜具有良好的抑制活性。秦苏佳等
[5]研究证实,植物乳杆菌CCFM8724的CFS可抑制变异链球菌与白色念珠菌双菌生物被膜形成;Kim等
[6]研究发现,从发酵食品中分离的短乳杆菌KCCM 202399的CFS对变异链球菌KCTC5458生物被膜具有抑制作用;Masebe等
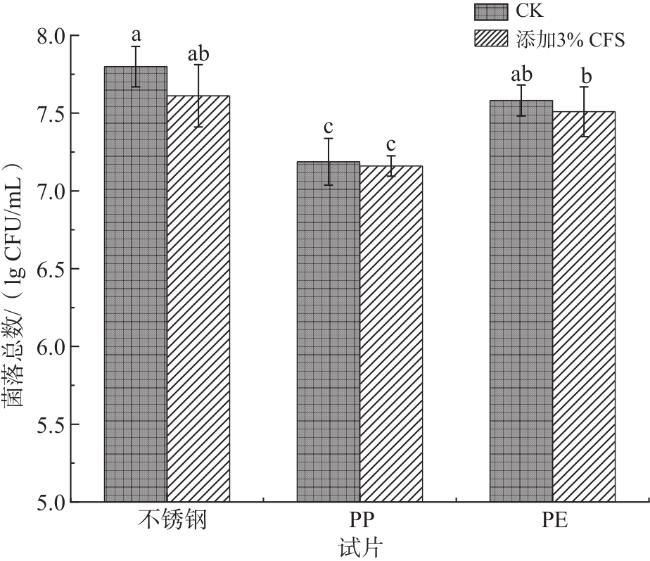
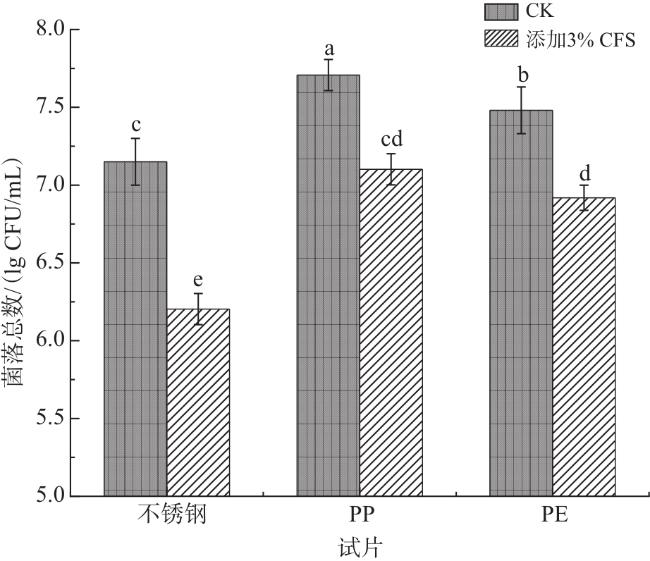
[7]研究发现,嗜酸乳杆菌La14 150B、植物乳植杆菌B411及鼠李糖乳杆菌ATCC 53103,对聚氯乙烯(PVC)和不锈钢表面的单增李斯特氏菌生物被膜均表现出不同程度的抑制活性。
希瓦氏菌是水产领域常见的优势腐败菌,易在物体表面形成生物被膜,对食品安全与人类健康存在潜在危害
[8]。目前,希瓦氏菌生物被膜的调控与抑制已引起广泛关注,但现有研究多聚焦于腐败希瓦氏菌,且生物被膜抑制剂相关报道以植物来源为主
[9-11]。海藻希瓦氏菌(
Shewanella algae)作为条件致病菌,广泛分布于海产品及海洋环境中,是希瓦氏菌属临床感染常见的病原体之一(占比达35.16%)
[12]。该菌可形成生物被膜并存在群体感应现象,然而关于乳酸菌对其生物被膜的抑制作用,目前尚未见相关报道。