1 材料与方法
1.1 仪器与试剂
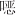 唑(SMX)、磺胺二甲基嘧啶(SMZ)、磺胺间甲氧嘧啶(SMM)、磺胺喹
唑(SMX)、磺胺二甲基嘧啶(SMZ)、磺胺间甲氧嘧啶(SMM)、磺胺喹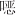 啉(SQ)、磺胺间二甲氧嘧啶(SDM)、磺胺嘧啶(SDZ)、磺胺噻唑(STZ)、磺胺甲基嘧啶(SMR)、磺胺二甲异
啉(SQ)、磺胺间二甲氧嘧啶(SDM)、磺胺嘧啶(SDZ)、磺胺噻唑(STZ)、磺胺甲基嘧啶(SMR)、磺胺二甲异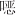 唑(SIZ)、磺胺甲噻二唑(SMTZ)、磺胺氯哒嗪(SCP)和磺胺多辛(SDX)。(2)氟喹诺酮类(8种),恩诺沙星(ENR)、环丙沙星(CIP)、氧氟沙星(OFX)、洛美沙星(LOM)、达氟沙星(DAN)、沙拉沙星(SAR)、培氟沙星(PEF)和诺氟沙星(NOR)。(3)酰胺醇类(4种),氯霉素(CAP)、甲砜霉素(TAP)、氟苯尼考(FF)和氟苯尼考胺(FFA)。准确移取各目标物标准品溶液,以甲醇定容至10 mL容量瓶,配制成1 μg/mL浓度的混合标准储备液。
唑(SIZ)、磺胺甲噻二唑(SMTZ)、磺胺氯哒嗪(SCP)和磺胺多辛(SDX)。(2)氟喹诺酮类(8种),恩诺沙星(ENR)、环丙沙星(CIP)、氧氟沙星(OFX)、洛美沙星(LOM)、达氟沙星(DAN)、沙拉沙星(SAR)、培氟沙星(PEF)和诺氟沙星(NOR)。(3)酰胺醇类(4种),氯霉素(CAP)、甲砜霉素(TAP)、氟苯尼考(FF)和氟苯尼考胺(FFA)。准确移取各目标物标准品溶液,以甲醇定容至10 mL容量瓶,配制成1 μg/mL浓度的混合标准储备液。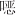 唑(SMX-D4)、磺胺二甲基嘧啶(SMZ-13C6)、磺胺间甲氧嘧啶(SMM-13C6)、磺胺喹
唑(SMX-D4)、磺胺二甲基嘧啶(SMZ-13C6)、磺胺间甲氧嘧啶(SMM-13C6)、磺胺喹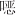 啉(SQ-13C6)、磺胺间二甲氧嘧啶(SDM-D6)、磺胺嘧啶(SDZ-D4)、磺胺噻唑(STZ-D4)、磺胺甲基嘧啶(SMR-13C6)、磺胺二甲异
啉(SQ-13C6)、磺胺间二甲氧嘧啶(SDM-D6)、磺胺嘧啶(SDZ-D4)、磺胺噻唑(STZ-D4)、磺胺甲基嘧啶(SMR-13C6)、磺胺二甲异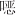 唑(SIZ-13C6)、磺胺甲噻二唑(SMTZ-13C6)、磺胺氯哒嗪(SCP-D3)、磺胺多辛(SDX-D6)。(2)氟喹诺酮类(8种),恩诺沙星(ENR-D5)、环丙沙星(CIP-D8)、氧氟沙星(OFX-D3)、洛美沙星(LOM-D5)、达氟沙星(DAN-D3)、沙拉沙星(SAR-D8)、培氟沙星(PEF-D5)、诺氟沙星(NOR-D5)。(3)酰胺醇类(4种),氯霉素(CAP-D5)、甲砜霉素(TAP-D3)、氟苯尼考(FF-D3)、氟苯尼考胺(FFA-D3)。准确移取各内标标准品溶液,以甲醇定容至10 mL容量瓶,配制成1 μg/mL浓度的同位素内标混合储备液。所有储备液均于-18 ℃避光条件下保存。
唑(SIZ-13C6)、磺胺甲噻二唑(SMTZ-13C6)、磺胺氯哒嗪(SCP-D3)、磺胺多辛(SDX-D6)。(2)氟喹诺酮类(8种),恩诺沙星(ENR-D5)、环丙沙星(CIP-D8)、氧氟沙星(OFX-D3)、洛美沙星(LOM-D5)、达氟沙星(DAN-D3)、沙拉沙星(SAR-D8)、培氟沙星(PEF-D5)、诺氟沙星(NOR-D5)。(3)酰胺醇类(4种),氯霉素(CAP-D5)、甲砜霉素(TAP-D3)、氟苯尼考(FF-D3)、氟苯尼考胺(FFA-D3)。准确移取各内标标准品溶液,以甲醇定容至10 mL容量瓶,配制成1 μg/mL浓度的同位素内标混合储备液。所有储备液均于-18 ℃避光条件下保存。1.2 试验方法
1.2.1 分析条件
表1 梯度洗脱程序 |
| 时间/min | 流动相A/% | 流动相B/% | 线性 |
|---|---|---|---|
| 0 | 90 | 10 | |
| 0.5 | 90 | 10 | 6 |
| 3 | 10 | 90 | 6 |
| 4 | 10 | 90 | 6 |
| 7 | 90 | 10 | 1 |
1.2.2 样品前处理
1.2.3 方法线性、检出限和定量限
1.2.4 回收率与精密度
2 结果与分析
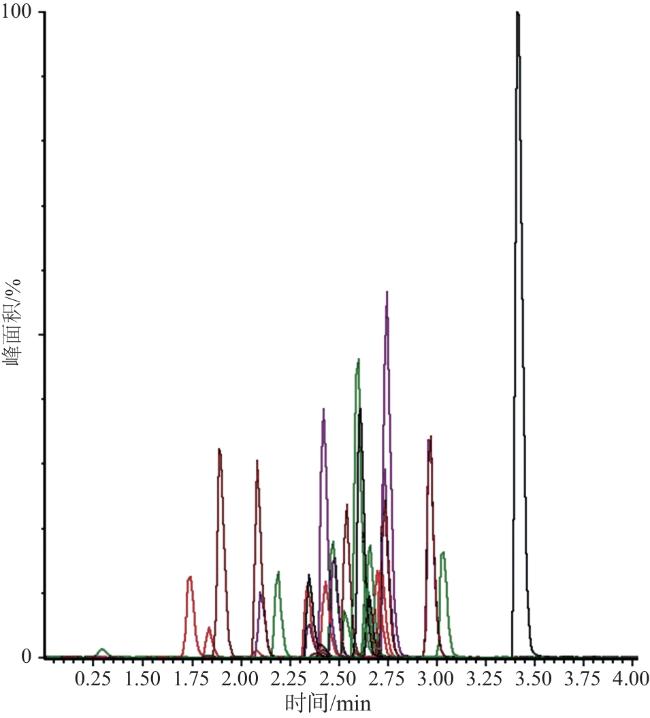
2.1 分析条件的优化
表2 24种化合物及内标物多反应监测条件(MRM) |
| 序号 | 药物 | 母离子/(m/z) | 子离子/ (m/z) | 锥孔电压/V | 碰撞能量/V |
|---|---|---|---|---|---|
| 1 | 磺胺噻唑 | 256.0 | 156.0/108.0 | 20/20 | 15/22 |
| 2 | 磺胺嘧啶 | 251.0 | 156.0/108.0 | 20/20 | 15/25 |
| 3 | 磺胺甲基嘧啶 | 265.0 | 156.0/172.0 | 20/20 | 15/15 |
| 4 | 磺胺二甲基嘧啶 | 279.1 | 186.0/92.0 | 20/20 | 15/30 |
| 5 | 磺胺甲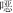 唑 唑 | 254.0 | 92.0/156.0 | 20/20 | 23/12 |
| 6 | 磺胺多辛 | 311.0 | 156.0/108.0 | 20/20 | 20/25 |
| 7 | 磺胺二甲异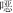 唑 唑 | 268.0 | 156.0/113.0 | 20/20 | 15/15 |
| 8 | 磺胺喹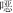 啉 啉 | 301.1 | 156.0/92.0 | 20/20 | 14/30 |
| 9 | 磺胺间甲氧嘧啶 | 281.1 | 156.0/92.0 | 20/20 | 17/30 |
| 10 | 磺胺间二甲氧嘧啶 | 311.0 | 156.0/92.0 | 20/20 | 18/30 |
| 11 | 磺胺氯哒嗪 | 285.0 | 156.0/108.0 | 20/20 | 15/25 |
| 12 | 磺胺甲噻二唑 | 271.0 | 156.0/108.0 | 20/20 | 15/25 |
| 13 | 环丙沙星 | 332.1 | 288.1/314.1 | 20/20 | 15/15 |
| 14 | 达氟沙星 | 358.2 | 82.2/340.1 | 20/20 | 34/10 |
| 15 | 恩诺沙星 | 360.3 | 316.2/342.1 | 20/20 | 20/20 |
| 16 | 沙拉沙星 | 386.1 | 299.1/342.1 | 20/20 | 28/15 |
| 17 | 培氟沙星 | 334.2 | 233.2/290.4 | 37/37 | 19/24 |
| 18 | 诺氟沙星 | 320.3 | 276.3/302.3 | 10/10 | 16/22 |
| 19 | 氧氟沙星 | 362.3 | 261.2/318.3 | 10/10 | 28/18 |
| 20 | 洛美沙星 | 352.3 | 265.2/308.3 | 10/10 | 25/16 |
| 21 | 氯霉素 | 321.0 | 152.0/257.0 | 30/30 | 20/10 |
| 22 | 甲砜霉素 | 353.9 | 185.1/290.0 | 30/30 | 20/10 |
| 23 | 氟苯尼考 | 355.8 | 119.1/335.9 | 30/30 | 20/10 |
| 24 | 氟苯尼考胺 | 248.1 | 130.0/230.0 | 35/35 | 22/12 |
| 25 | 磺胺噻唑-D4 | 260.0 | 160.0 | 20 | 15 |
| 26 | 磺胺嘧啶-D4 | 255.0 | 160.0 | 20 | 15 |
| 27 | 磺胺甲基嘧啶-13C6 | 271.0 | 162.0 | 20 | 15 |
| 28 | 磺胺二甲基嘧啶-13C6 | 285.2 | 186.0 | 32 | 16 |
| 29 | 磺胺甲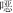 唑-D4 唑-D4 | 258.2 | 160.0 | 26 | 16 |
| 30 | 磺胺多辛-D6 | 314.0 | 156.0 | 20 | 18 |
| 31 | 磺胺二甲异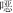 -13C6 -13C6 | 274.0 | 162.0 | 20 | 15 |
| 32 | 磺胺喹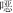 啉-13C6 啉-13C6 | 307.2 | 162.0 | 28 | 16 |
| 33 | 磺胺间甲氧嘧啶-13C6 | 287.2 | 162.0 | 28 | 18 |
| 34 | 磺胺间二甲氧嘧-D6 | 317.3 | 92.1 | 54 | 32 |
| 35 | 磺胺氯哒嗪-D3 | 314.0 | 156.0 | 20 | 18 |
| 36 | 磺胺甲噻二唑-13C6 | 277.0 | 162.0 | 20 | 15 |
| 37 | 环丙沙星-D8 | 340.2 | 296.2 | 19 | 15 |
| 38 | 达氟沙星-D3 | 361.2 | 343.2 | 20 | 20 |
| 39 | 恩诺沙星-D5 | 365.2 | 245.1 | 20 | 25 |
| 40 | 沙拉沙星-D8 | 384.2 | 303.2 | 20 | 25 |
| 41 | 培氟沙星-D5 | 339.1 | 321.1 | 20 | 18 |
| 42 | 诺氟沙星-D5 | 325.2 | 307.1 | 20 | 18 |
| 43 | 氧氟沙星-D3 | 365.2 | 261.0 | 10 | 25 |
| 44 | 洛美沙星-D5 | 357.2 | 270.2 | 20 | 8 |
| 45 | 氯霉素-D5 | 325.9 | 157.2 | 30 | 18 |
| 46 | 甲砜霉素-D3 | 357.1 | 188.0 | 20 | 20 |
| 47 | 氟苯尼考-D3 | 359.0 | 339.0 | 20 | 5 |
| 48 | 氟苯尼考胺-D3 | 251.2 | 130.0 | 35 | 20 |
2.2 方法线性、检出限和定量限
表3 24种化合物回归方程及相关系数 |
| 序号 | 药物 | 回归方程 | 相关系数(R2 ) | 检出限/(ng/mL) | 定量限/(ng/mL) |
|---|---|---|---|---|---|
| 1 | 磺胺噻唑 | y=0.228 838x-0.047 809 1 | 0.998 082 | 0.12 | 0.36 |
| 2 | 磺胺嘧啶 | y=0.191 854x-0.016 234 8 | 0.996 401 | 0.02 | 0.06 |
| 3 | 磺胺甲基嘧啶 | y=0.225 554x-0.033 521 3 | 0.991 440 | 0.05 | 0.16 |
| 4 | 磺胺二甲基嘧啶 | y=0.236 559x-0.035 562 5 | 0.995 602 | 0.04 | 0.12 |
| 5 | 磺胺甲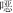 唑 唑 | y=0.239 951x-0.046 873 1 | 0.994 501 | 0.12 | 0.36 |
| 6 | 磺胺多辛 | y=0.207 532x-0.034 590 9 | 0.996 790 | 0.03 | 0.09 |
| 7 | 磺胺二甲异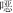 唑 唑 | y=0.226 76x-0.055 629 5 | 0.995 263 | 0.07 | 0.20 |
| 8 | 磺胺喹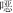 啉 啉 | y=0.586 744x-0.044 223 6 | 0.995 963 | 0.05 | 0.14 |
| 9 | 磺胺间甲氧嘧啶 | y=0.293 464x-0.044 914 1 | 0.994 858 | 0.07 | 0.21 |
| 10 | 磺胺间二甲氧嘧啶 | y=0.696 854x-0.053 219 5 | 0.999 899 | 0.30 | 0.90 |
| 11 | 磺胺氯哒嗪 | y=0.215 554x-0.025 586 5 | 0.993 555 | 0.05 | 0.15 |
| 12 | 磺胺甲噻二唑 | y=0.225 654x-0.059 325 8 | 0.994 156 | 0.06 | 0.19 |
| 13 | 环丙沙星 | y=0.402 043x+0.442 194 | 0.994 054 | 0.20 | 0.60 |
| 14 | 达氟沙星 | y=0.076 103 7x+0.421 517 | 0.998 662 | 0.10 | 0.30 |
| 15 | 恩诺沙星 | y=0.437 429x+0.702 566 | 0.998 440 | 0.13 | 0.39 |
| 16 | 沙拉沙星 | y=0.575 35x+1.017 94 | 0.993 139 | 0.15 | 0.45 |
| 17 | 培氟沙星 | y=0.314 479x+0.420 461 | 0.993 164 | 0.29 | 0.87 |
| 18 | 诺氟沙星 | y=0.126 463x+0.118 325 | 0.992 182 | 1.00 | 3.00 |
| 19 | 氧氟沙星 | y=0.611 955x+0.814 736 | 0.991 368 | 0.12 | 0.36 |
| 20 | 洛美沙星 | y=0.278 878x+0.262 32 | 0.993 188 | 0.13 | 0.39 |
| 21 | 氯霉素 | y=0.229 526x+0.010 186 4 | 0.991 107 | 0.05 | 0.15 |
| 22 | 甲砜霉素 | y=0.184 384x+0.010 775 5 | 0.993 387 | 0.26 | 0.78 |
| 23 | 氟苯尼考 | y=0.212 149x+0.007 989 3 | 0.996 321 | 0.20 | 0.60 |
| 24 | 氟苯尼考胺 | y=0.225 414x+0.005 340 48 | 0.995 746 | 0.24 | 0.72 |
2.3 准确度和精密度
表4 水体中24种药物的回收率和RSD(n=7) |
| 序 号 | 药物名称 | 添加水平/ (1.0 ng/mL) | 添加水平/ (5.0 ng/mL) | 添加水平/(10.0 ng/mL) | |||
|---|---|---|---|---|---|---|---|
| 回收率 /% | RSD /% | 回收率 /% | RSD /% | 回收率 /% | RSD /% | ||
| 1 | 磺胺噻唑 | 105.1 | 7.3 | 103.9 | 8.9 | 106.5 | 3.5 |
| 2 | 磺胺嘧啶 | 106.1 | 6.6 | 101.1 | 1.7 | 106.6 | 3.5 |
| 3 | 磺胺甲基嘧啶 | 110.9 | 5.4 | 98.1 | 8.1 | 110.8 | 3.3 |
| 4 | 磺胺二甲基嘧啶 | 105.5 | 3.8 | 100.6 | 3.3 | 107.5 | 2.9 |
| 5 | 磺胺甲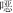 唑 唑 | 112.0 | 6.1 | 92.3 | 6.9 | 110.5 | 2.7 |
| 6 | 磺胺多辛 | 100.7 | 6.5 | 96.4 | 2.1 | 107.6 | 3.9 |
| 7 | 磺胺二甲异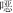 唑 唑 | 109.9 | 4.2 | 96.6 | 2.7 | 107.0 | 5.4 |
| 8 | 磺胺喹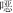 啉 啉 | 91.3 | 8.9 | 97.3 | 5.0 | 104.5 | 3.4 |
| 9 | 磺胺间甲氧嘧啶 | 110.9 | 3.8 | 94.3 | 4.1 | 109.4 | 3.9 |
| 10 | 磺胺间二甲氧嘧啶 | 88.1 | 6.3 | 108.0 | 2.2 | 96.0 | 2.9 |
| 11 | 磺胺氯哒嗪 | 107.5 | 8.9 | 100.4 | 2.4 | 109.3 | 4.5 |
| 12 | 磺胺甲噻二唑 | 97.0 | 3.7 | 97.0 | 1.9 | 103.5 | 4.4 |
| 13 | 环丙沙星 | 88.4 | 7.3 | 102.3 | 7.4 | 108.1 | 5.7 |
| 14 | 达氟沙星 | 105.5 | 2.1 | 102.0 | 4.3 | 109.4 | 5.7 |
| 15 | 恩诺沙星 | 87.0 | 8.4 | 100.4 | 3.6 | 106.8 | 3.1 |
| 16 | 沙拉沙星 | 88.0 | 5.4 | 94.6 | 4.6 | 101.1 | 5.2 |
| 17 | 培氟沙星 | 85.9 | 5.5 | 95.7 | 6.8 | 100.9 | 5.5 |
| 18 | 诺氟沙星 | 88.2 | 3.1 | 95.7 | 5.8 | 100.9 | 9.6 |
| 19 | 氧氟沙星 | 107.7 | 5.9 | 101.8 | 4.1 | 108.4 | 3.8 |
| 20 | 洛美沙星 | 87.4 | 6.1 | 92.7 | 6.0 | 97.7 | 7.7 |
| 21 | 氯霉素 | 106.9 | 5.8 | 105.3 | 4.1 | 97.2 | 4.4 |
| 22 | 甲砜霉素 | 91.0 | 2.8 | 98.2 | 3.6 | 96.3 | 6.2 |
| 23 | 氟苯尼考 | 94.2 | 5.6 | 98.1 | 4.6 | 94.3 | 4.1 |
| 24 | 氟苯尼考胺 | 97.8 | 3.4 | 113.8 | 3.8 | 97.4 | 1.9 |