1 UV-B辐射对植物形态及生长发育的影响
1.1 形态发育调控
1.2 细胞膜系统稳定性
1.3 渗透调节
1.4 抗氧化防御
1.5 次生代谢
1.6 光合作用
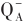 向
向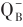 传递过程受阻,致使快还原型库PQ受影响。由此表明,适量UV-B辐射有益于植物叶片叶绿素的合成,从而增强光合作用;而UV-B辐射持续时间或强度超过阈值时,植物PS Ⅱ最大光化学效率受损,影响叶绿素和光合蛋白复合体的合成,进而抑制植物的光合作用。
传递过程受阻,致使快还原型库PQ受影响。由此表明,适量UV-B辐射有益于植物叶片叶绿素的合成,从而增强光合作用;而UV-B辐射持续时间或强度超过阈值时,植物PS Ⅱ最大光化学效率受损,影响叶绿素和光合蛋白复合体的合成,进而抑制植物的光合作用。
安徽农学通报 >
2025 , Vol. 31 >Issue 8: 41 - 48
DOI: https://doi.org/10.16377/j.cnki.issn1007-7731.2025.08.011
UV-B胁迫下植物的生理适应及分子应答
|
张 菲(1997—),女,四川绵阳人,硕士研究生,从事牧草种质抗逆研究。 |
Copy editor: 何艳
收稿日期: 2024-07-09
网络出版日期: 2025-04-28
基金资助
四川省科技计划-科技创新人才项目(2023JDRC0040)
林草科技创新发展研究项目(2023132016)
Physiological adaptations and molecular responses of plants under UV-B stress
Received date: 2024-07-09
Online published: 2025-04-28
中波紫外线(UV-B)辐射作为非生物胁迫因子,对植物的形态发育、生理生化过程及分子机制产生显著影响。本文综述了UV-B辐射对植物形态的调控作用(如抑制茎伸长、减小叶面积、改变根冠比等),以及其对细胞膜系统稳定性、渗透调节物质(可溶性糖、脯氨酸等)、抗氧化防御系统(SOD、CAT、APX等酶活性及非酶类抗氧化剂)和光合系统的直接或间接损伤。植物通过合成类黄酮、花青素等次生代谢物、激活UVR8介导的信号通路以及激活激素调控与次生代谢基因等分子机制,增强对UV-B胁迫的适应性。此外,UV-B与其他环境因子(如温度、干旱、重金属)的复合胁迫常表现出协同或拮抗效应,其作用机制复杂且因物种而异。当前研究多集中于农作物和草本植物,且研究条件多局限于人工环境,未来需结合多组学技术与野外长期观测,深入解析植物响应UV-B辐射的分子网络及其生态适应性,为抗逆育种和生态修复提供参考。
张菲 , 李英主 , 杜鹏飞 , 白史且 , 鄢家俊 . UV-B胁迫下植物的生理适应及分子应答[J]. 安徽农学通报, 2025 , 31(8) : 41 -48 . DOI: 10.16377/j.cnki.issn1007-7731.2025.08.011
As an abiotic stress factor, UV-B radiation significantly impacts plant morphological development, physiological and biochemical processes, and molecular mechanisms. This paper reviewed the regulatory effects of UV-B radiation on plant morphology (e.g., inhibition of stem elongation, reduction in leaf area, and alteration of root-to-shoot ratio), as well as its direct or indirect damage to cell membrane stability, osmotic regulation substances (e.g., soluble sugars, proline), antioxidant defense systems (enzyme activities such as SOD, CAT, APX, and non-enzymatic antioxidants), and photosynthetic systems. Plants enhance their adaptability to UV-B stress through molecular mechanisms such as synthesizing secondary metabolites like flavonoids and anthocyanins, activating the UVR8-mediated signaling pathway, and activating hormone regulation and secondary metabolic genes. Furthermore, combined stress from UV-B and other environmental factors (e.g., temperature, drought, heavy metals) often exhibits synergistic or antagonistic effects, with complex mechanisms varying across species. Current research primarily focuses on crops and herbaceous plants under controlled experimental conditions. Future studies should integrate multi-omics technologies and long-term field observations to deeply unravel the molecular networks and ecological adaptability of plants in response to UV-B radiation, providing insights for stress-resistant breeding and ecological restoration.
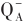 向
向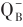 传递过程受阻,致使快还原型库PQ受影响。由此表明,适量UV-B辐射有益于植物叶片叶绿素的合成,从而增强光合作用;而UV-B辐射持续时间或强度超过阈值时,植物PS Ⅱ最大光化学效率受损,影响叶绿素和光合蛋白复合体的合成,进而抑制植物的光合作用。
传递过程受阻,致使快还原型库PQ受影响。由此表明,适量UV-B辐射有益于植物叶片叶绿素的合成,从而增强光合作用;而UV-B辐射持续时间或强度超过阈值时,植物PS Ⅱ最大光化学效率受损,影响叶绿素和光合蛋白复合体的合成,进而抑制植物的光合作用。| 1 |
|
| 2 |
|
| 3 |
|
| 4 |
|
| 5 |
|
| 6 |
张红霞,吴能表,胡丽涛,等. 不同强度UV-B辐射胁迫对蚕豆幼苗生长及叶绿素荧光特性的影响[J]. 西南师范大学学报(自然科学版),2010,35(1):105-110.
|
| 7 |
|
| 8 |
|
| 9 |
王小文. GhNAC1调控棉花耐盐性的机理研究[D]. 济南:山东师范大学,2023.
|
| 10 |
韩发,朱文琰,师生波,等. 模拟增加UV-B辐射对青藏高原四种植物形态特征和生理机制的影响[C]//三江源区生态保护与可持续发展高级学术研讨会论文摘要汇编. 西宁,2005:73.
|
| 11 |
刘茜,刘博文,王洋,等. UV-B辐射对不同生态型垂穗披碱草幼苗生长和抗氧化酶系统的影响[J]. 草地学报,2019,27(4):898-905.
|
| 12 |
徐佳妮,雷梦琦,鲁瑞琪,等. UV-B辐射增强对植物影响的研究进展[J]. 基因组学与应用生物学,2015,34(6):1347-1352.
|
| 13 |
|
| 14 |
梁泰帅,赵肖琼,陈乐,等. 外源DA-6对UV-B辐射胁迫下紫花苜蓿幼苗生长调节及花青素合成代谢的影响[J]. 黑龙江畜牧兽医,2023(12):107-113,124.
|
| 15 |
邱文静,陈仕勇,罗鑫,等. 野生垂穗披碱草种质资源UV-B抗性综合评价[J]. 草地学报,2022,30(5):1194-1202.
|
| 16 |
陈甜甜,税贤,钱敏杰,等.增强UV-B辐射对“台农一号”杧果果实品质及其抗氧化酶防御系统的影响[J].中国南方果树,2024,53(6):114-123,130.
|
| 17 |
习亚君. 紫花苜蓿氧化/抗氧化代谢对不同水平UV-B胁迫的响应[D]. 临汾:山西师范大学,2022.
|
| 18 |
|
| 19 |
赵媛媛. UV-B辐射和干旱胁迫对白沙蒿形态及生理的影响[D]. 兰州:兰州大学,2017.
|
| 20 |
王红,岳堃,郭钰柬,等. UV-B辐射诱导芒果叶片抗氧化响应研究[J]. 热带亚热带植物学报,2020,28(1):70-77.
|
| 21 |
拉本,胡娟,张旭萍. 干旱胁迫对植物生理的影响以及分子机制的响应研究进展[J]. 青海草业,2022,31(4):31-35.
|
| 22 |
|
| 23 |
黄志慧,张一宁,李娜娜,等.增补UV-B辐射对菥蓂生理特性及次生代谢产物的影响[J].植物研究,2022,42(6):1079-1087.
|
| 24 |
陈艳,张文娟,邓昌蓉,等. UV-B辐射对不同发育时期辣椒主要果实品质的影响[J]. 华北农学报,2023,38():180-187.
|
| 25 |
薛盈文,黄寿光,范博文,等. 低温和UV-B复合胁迫对小麦幼苗抗氧化酶和渗透调节物质的影响[J]. 麦类作物学报,2017,37(6):834-840.
|
| 26 |
唐莉娜,林文雄,梁义元,等. UV-B辐射增强对水稻蛋白质及核酸的影响研究[J]. 中国生态农业学报,2004,12(1):40-42.
|
| 27 |
王玲丽,周晓君,刘文哲. 增强UV-B辐射对喜树生理指标及喜树碱含量的影响(英文)[J]. 西北植物学报,2016,36(5):979-986.
|
| 28 |
邵建平,杨志新,何承刚,等. 增强UV-B辐射对2个烤烟品种生理代谢指标的影响[J]. 热带作物学报,2015,36(1):132-137.
|
| 29 |
吴贡萍,阿力日坡,张雅洁,等. 老芒麦抗逆性评价研究进展[J]. 草学,2024(2):37-44.
|
| 30 |
|
| 31 |
谢博勋. 两种罗布麻响应UV-B胁迫的转录组学及代谢组学分析[D]. 银川:宁夏大学,2022.
|
| 32 |
|
| 33 |
|
| 34 |
任举. UV-B补光灯对茄子幼苗生长、抗性生理及抗病性的影响[J]. 西北园艺,2024(5):48-52.
|
| 35 |
赵欣悦,湛东武,周富亮,等.中波紫外线辐照对甜玉米种子萌发的影响及转录组分析[J].西北农林科技大学学报(自然科学版),2024,52(11):1-12.
|
| 36 |
吕杰,王超,刘璐,等. UV-B胁迫对植物抗氧化酶活性的影响[J]. 吉林师范大学学报(自然科学版),2019,40(4):113-117.
|
| 37 |
刘英,于雪莹,于莉莉,等. UV-B辐射下不同树龄杜仲叶片光合及部分生理特性的变化[J]. 东北林业大学学报,2020,48(6):42-46,50.
|
| 38 |
褚润,陈年来,韩国君,等. 三种UV-B辐射强度下香蒲的生长和抗氧化状况[J]. 湿地科学,2020,18(1):32-39.
|
| 39 |
|
| 40 |
|
| 41 |
兰孟焦,后猛,肖满秋,等. AP2/ERF转录因子参与植物次生代谢和逆境胁迫响应的研究进展[J]. 植物遗传资源学报,2023,24(5):1223-1235.
|
| 42 |
马宗桓. 光照强度对葡萄果实品质及花青苷合成的调控机理研究[D]. 兰州:甘肃农业大学,2019.
|
| 43 |
|
| 44 |
郝婧玮,梅念念,渠利霞,等. UV-B对红豆杉不同提取方式紫杉醇含量的影响[J]. 江苏农业科学,2019,47(21):266-269.
|
| 45 |
沈甜,牛锐敏,许泽华,等. UV-B照射时长对酿酒葡萄果实品质及类黄酮代谢产物的影响[J]. 食品工业科技,2024,45(17):73-82.
|
| 46 |
王园,党悦方,张典,等. 夏枯草幼苗中有效成分与生理指标对增强UV-B辐射的动态响应[J]. 西北大学学报(自然科学版),2017,47(3):414-421.
|
| 47 |
张亚丽,王引权,杨彩霞. 紫外线-B辐射增强对药用植物生理生化影响研究进展[J]. 甘肃中医药大学学报,2019,36(4):83-87.
|
| 48 |
盛建军,李想,何永美,等. UV-B辐射对花青素合成代谢的影响及分子机理[J]. 植物生理学报,2019,55(7):949-958.
|
| 49 |
|
| 50 |
|
| 51 |
杨玉皎,郭淑萍,杨顺林,等. 增强UV-B辐射对杧果叶片光合生理和超显微结构的影响[J]. 果树学报,2021,38(9):1524-1539.
|
| 52 |
师生波,尚艳霞,师瑞,等. 高山植物美丽风毛菊PS II光化学效率和光合色素对短期增补UV-B辐射的响应[J]. 植物生态学报,2012,36(5):420-430.
|
| 53 |
|
| 54 |
王林叶,吉冰璇,曾彦达,等. 增强UV-B辐射对光氧化水稻812HS光合特性和生长的影响[J]. 核农学报,2020,34(5):913-920.
|
| 55 |
李良博,唐天向,海梅荣,等. 植物对UV-B辐射增强的响应及其分子机制[J]. 中国农学通报,2015,31(13):159-163.
|
| 56 |
何文兴. 高寒植物对低温和强UV-B辐射胁迫响应的分子机制研究[D]. 成都:四川大学,2005.
|
| 57 |
|
| 58 |
|
| 59 |
|
| 60 |
王丽霞. 植物紫外光受体UVR8介导UV-B信号转导的分子机制研究 [D].武汉:华中农业大学, 2023.
|
| 61 |
|
| 62 |
|
| 63 |
|
| 64 |
凌成婷,李想,周应嫄,等. UV-B辐射调控的植物激素路径和分子响应[J]. 植物生理学报,2021,57(10):1839-1851.
|
| 65 |
|
| 66 |
|
| 67 |
|
| 68 |
韩超,申海玉,刘庆. 云杉幼苗对气候变暖和UV-B辐射增强的光合响应[J]. 西北植物学报,2014,34(4):820-827.
|
| 69 |
郭晓瑞,汪红玲,王化楠,等. 增强UV-B辐射及氮水平对长春花生长和生理代谢的影响[J]. 植物研究,2011,31(5):592-596.
|
| 70 |
张来军,贾敬芬,梅康,等. 褪黑素对秦艽原生质体抗UV-B环境胁迫的作用[J]. 核农学报,2015,29(5):830-835.
|
| 71 |
胡正华,索福喜,赵晓莉,等. UV-B增加与酸雨复合处理对大豆种子萌发和幼苗生长的影响[J]. 生态环境,2005,14(4):523-525.
|
| 72 |
高潇潇,高召华,陈建军,等. 增强UV-B辐射和接种稻瘟病菌对2个水稻品种幼苗叶片3个生理指标的影响[J]. 植物资源与环境学报,2010,19(1):56-62.
|
/
| 〈 |
|
〉 |