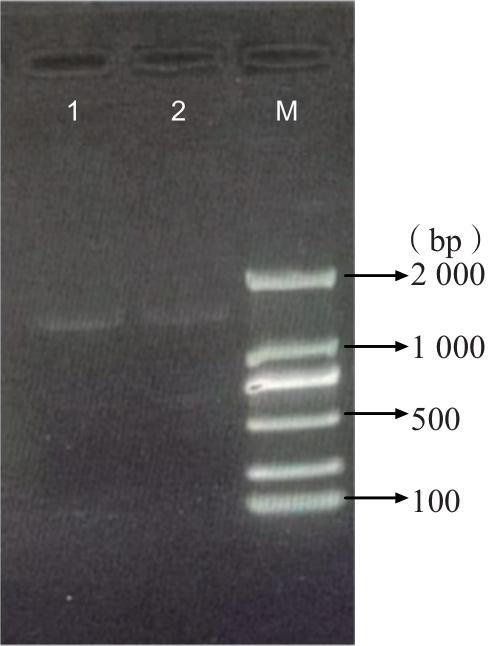
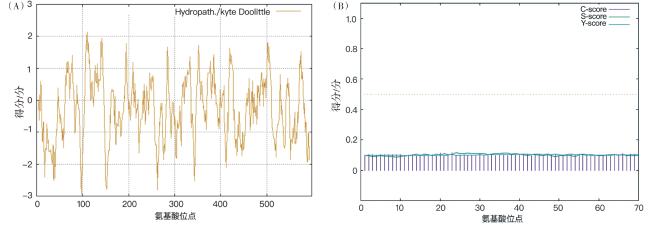
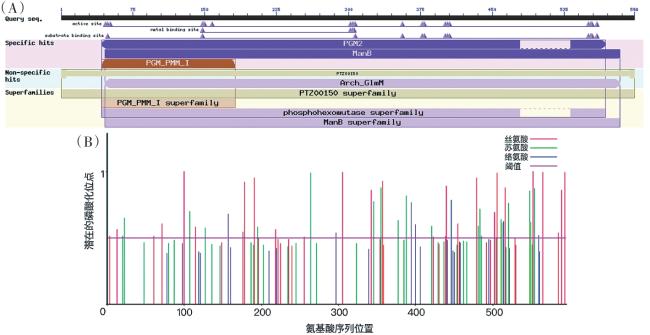
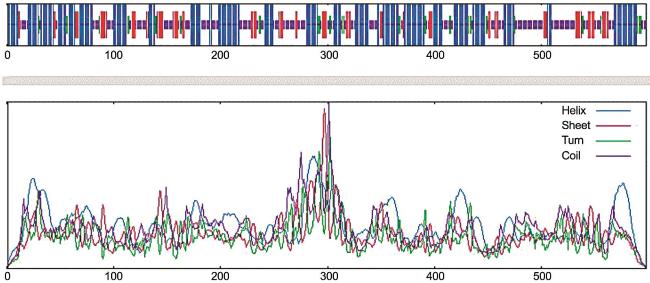
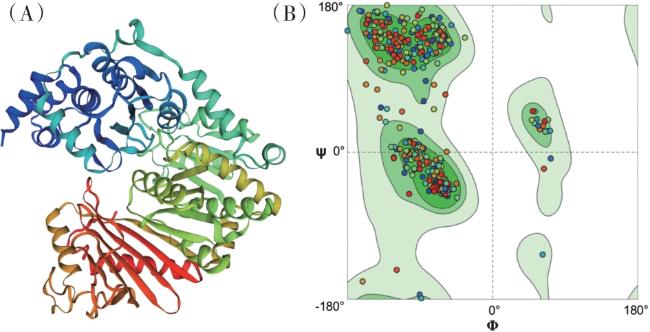
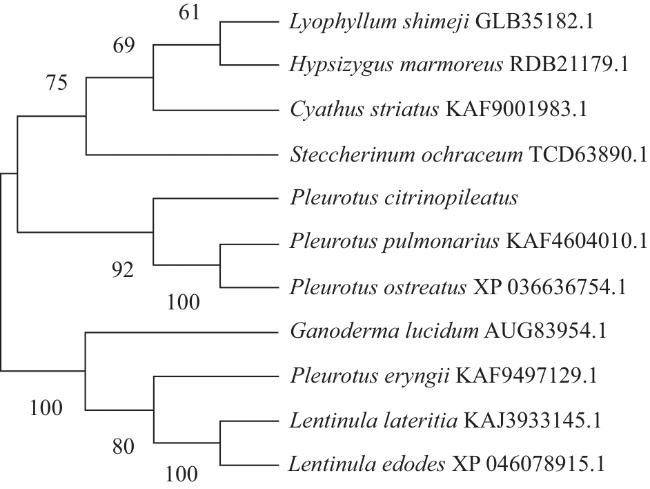
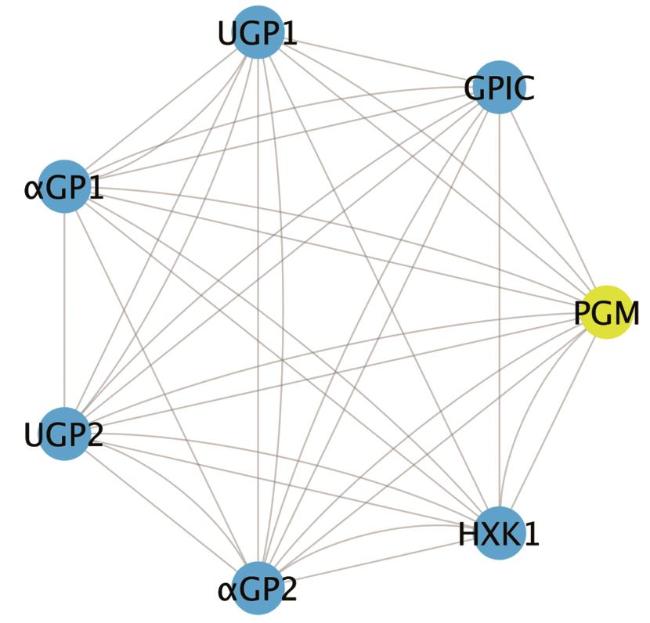
To explore the characteristics and structure of the phosphoglucomutase (PGM) gene in Pleurotus citrinopileatus, the study was based on the genomic data of Pleurotus citrinopileatus. The PGM gene was cloned by RT-PCR technology, and the encoded protein was analyzed by bioinformatics, including physicochemical properties, hydrophobicity, secondary and tertiary structures, etc. The results showed that the full length sequence of the PGM gene in P. citrinopileatus was 1 797 bp, encoding 598 amino acids, with a molecular weight of 66.35 kDa. The isoelectric point of the protein was 5.98, the average hydrophilicity was -0.278, and the instability index was 29.54, indicating that it was an acidic, hydrophilic and stable protein. The protein had no signal peptide, no cleavage site, and no transmembrane helices, belonging to a non-secreted and non-transmembrane protein. There were conserved domains in the amino acid sequence regions, belonging to the PTZ00150 gene family, with 81 phosphorylation sites, located in the cytoplasm. The secondary structure mainly includes α-helices (43.14%), irregular curls (35.79%), extended chains (14.72%), and β-folds (6.35%); the tertiary structure is mainly composed of alpha helices and irregular coils, and the structure is relatively stable. The results of homology and phylogenetic tree analysis showed that the similarity of PcPGM with Pleurotus ostreatus, Pleurotus pulmonarius, Hypsizygus marmoreus and Lyophyllum shimeji was 78.04%, 79.7%, 71.33% and 67.50%, respectively, and it was most closely related to P. ostreatus and P. pulmonarius, both belonging to the Auriculariaceae family. There were 6 proteins that might interact with the PcPGM protein, including hexokinase 1 (HXK1), glucose-6-phosphate isomerase (GPIC), α-glucan phosphorylase 1 (αGP1), αGP2, UTP-glucose-1-phosphate uridylyltransferase 1 (UGP1) and UGP2, all of which were related to sugar metabolism. This study provides a reference for further exploration of the biological function and medicinal value of the PGM gene in P. citrinopileatus.