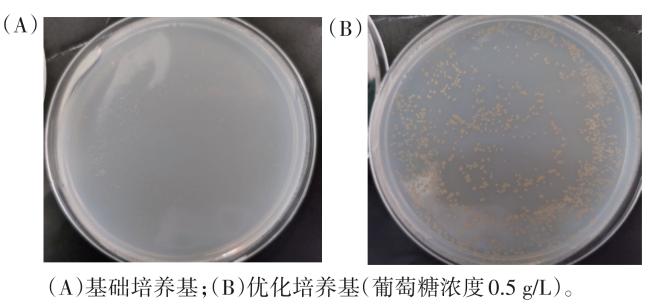
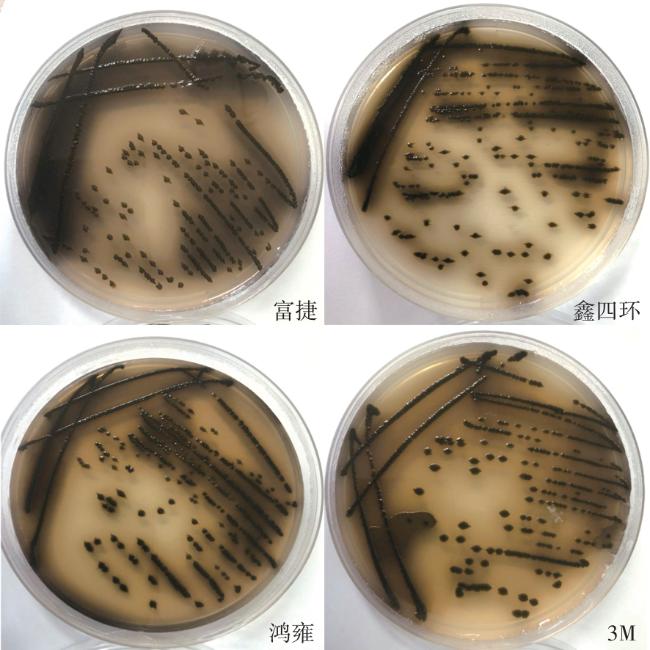
To screen the tyrosine medium formula that could make Bacillus subtilis var. niger produce melanin stably, the tyrosine medium was optimized by single factor experiment method, and the effects of Tyrosine (L-tyrosine, 0, 0.5, 1.0, 2.0 and 3.0 g/L, respectively), carbon source (glucose, 0, 0.5, 1.0, 2.0 and 3.0 g/L, respectively), nitrogen source (tryptone, 1.0, 2.0 and 3.0 g/L, respectively),amino acid (casein,0, 10.0, 20.0, 40.0 and 60.0 mL/L, respectively) and induction time (24, 48, 72 and 96 h) on the production of melanin by Bacillus subtilis var. niger were investigated. The adaptability of 4 kinds of indicators, including ATCC 9372 biological indicator sterilized by Fujie brand ethylene oxide, was verified. The results showed that the optimal addition amounts of L-tyrosine, glucose, tryptone and casein were 0.5, 0.5, 0.5 g/L and 10 mL/L, respectively. The optimal culture time was 72~96 h. Under this condition, the Bacillus subtilis var. niger could be induced well, and the melanin produced was stable. The results provided a reference for the screening, culture and further application of Bacillus subtilis var. niger.