1 材料与方法
1.1 样品配制信息
1.2 实验动物
1.3 试剂与仪器
1.4 测定指标和方法
1.4.1 最大耐受浓度(MTC)
1.4.2 调节气血
1.4.3 调节免疫力
1.5 数据处理
2 结果与分析
2.1 人参阿胶口服液调节气血的MTC测算
表1 人参阿胶口服液改善贫血功效的MTC |
| 组别 | 人参阿胶口服液浓度/(μL/mL) | 死亡数/尾 | 死亡率/% | 表型 |
|---|---|---|---|---|
| 正常对照组 | 0 | 0 | 0 | 未见明显异常 |
| 模型对照组 | 0 | 0 | 0 | 未见明显异常 |
| 人参阿胶口服液组 | 7.81 | 0 | 0 | 与模型对照组状态相似 |
| 15.60 | 0 | 0 | 与模型对照组状态相似 | |
| 31.20 | 0 | 0 | 与模型对照组状态相似 | |
| 62.50 | 11 | 37 | 较模型对照组状态差 | |
| 125.00 | 14 | 47 | 较模型对照组状态差 |
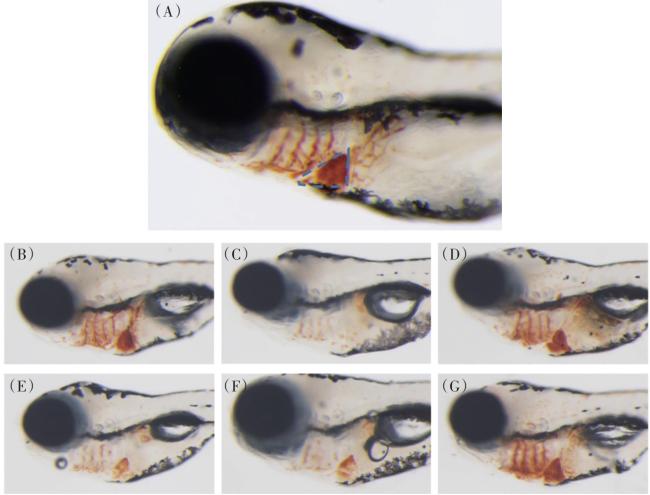
2.2 人参阿胶口服液调节气血评价
表2 人参阿胶口服液改善贫血功效评价 |
| 组别 | 浓度 | 心脏红细胞染色强度(像素) |
|---|---|---|
| 正常对照组 | 4 936 ± 114.00*** | |
| 模型对照组 | 779 ± 29.40 | |
| 阳性对照组 | 250.00 μg/mL | 4 956 ± 94.10*** |
| 人参阿胶口服液组 | 7.81 µL/mL | 2 182 ± 132.00 |
| 15.60 µL/mL | 2 934 ± 209.00** | |
| 31.20 µL/mL | 5 223 ± 92.90*** |
|
2.3 人参阿胶口服液调节免疫力MTC测算
表3 人参阿胶口服液增强免疫力功效的MTC |
| 组别 | 人参阿胶口服液浓度/(μL/mL) | 死亡数/尾 | 死亡率/% | 表型 |
|---|---|---|---|---|
| 正常对照组 | 0 | 0 | 0 | 未见明显异常 |
| 模型对照组 | 0 | 0 | 0 | 未见明显异常 |
| 人参阿胶口服液组 | 0.98 | 0 | 0 | 与模型对照组状态相似 |
| 1.95 | 0 | 0 | 与模型对照组状态相似 | |
| 3.91 | 0 | 0 | 与模型对照组状态相似 | |
| 7.81 | 3 | 10 | 较模型对照组状态差 | |
| 15.60 | 18 | 60 | 较模型对照组状态差 |
2.4 人参阿胶口服液调节免疫力评价
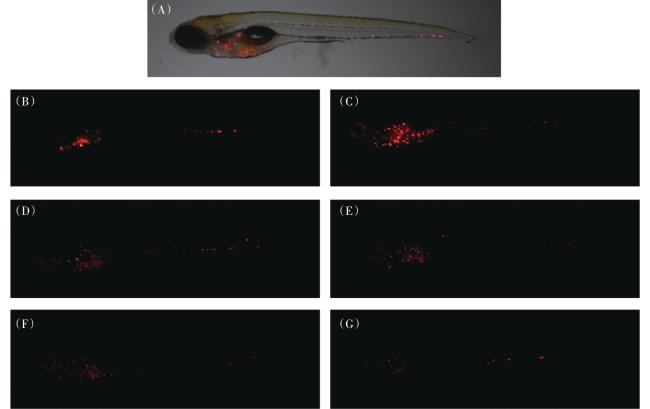
2.4.1 促进巨噬细胞吞噬
表4 人参阿胶口服液促进巨噬细胞吞噬功效评价 |
| 组别 | 浓度 | 斑马鱼体内剩余荧光颗粒数量/个 |
|---|---|---|
| 正常对照组 | 22.00 ± 0.91*** | |
| 模型对照组 | 42.80 ± 1.09 | |
| 阳性对照组 | 125.00 μg/mL | 29.10 ± 0.57*** |
| 人参阿胶口服液组 | 0.98 µL/mL | 28.10 ± 1.10*** |
| 1.95 µL/mL | 25.50 ± 0.82*** | |
| 3.91 µL/mL | 20.50 ± 0.91*** |
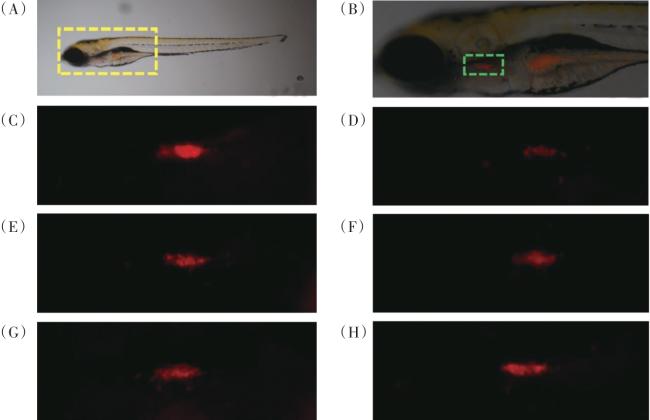
2.4.2 增强T细胞
表5 人参阿胶口服液增强T细胞功效 |
| 组别 | 浓度 | T细胞荧光强度(像素) |
|---|---|---|
| 正常对照组 | 32 111 ± 1279*** | |
| 模型对照组 | 11 049 ± 1043 | |
| 阳性对照组 | 125.00 μg/mL | 19 387 ± 908*** |
| 人参阿胶口服液 | 0.98 µL/mL | 17 848 ± 1272 |
| 1.95 µL/mL | 23 229 ± 630*** | |
| 3.91 µL/mL | 25 075 ± 1316*** |