1 材料与方法
1.1 主要试剂及仪器
1.2 试验设计
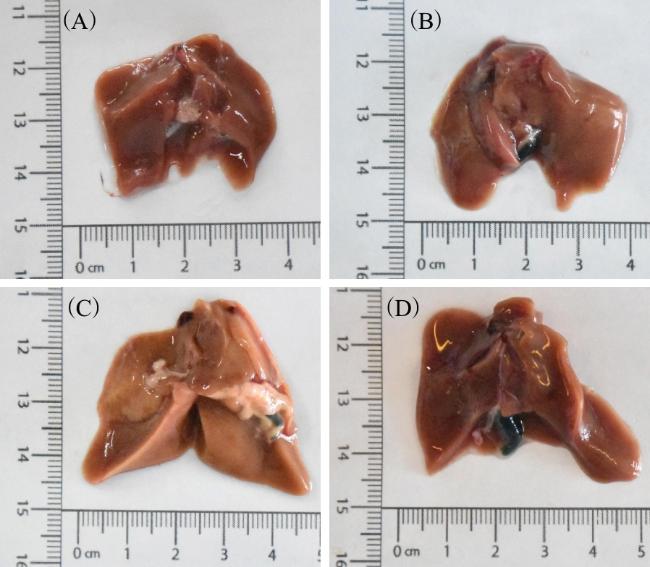
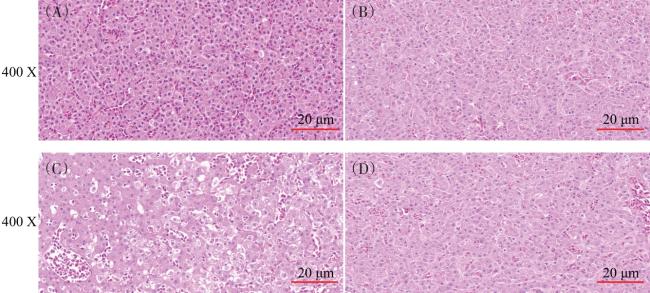
1.3 鹌鹑肝脏的解剖学和组织病理学观察
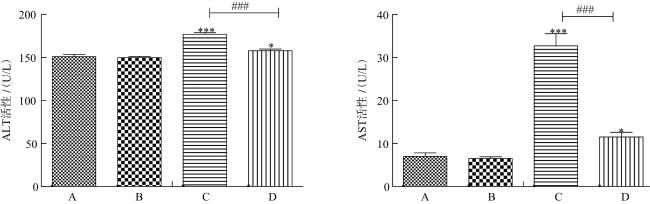
1.4 鹌鹑血清生化肝功能指标
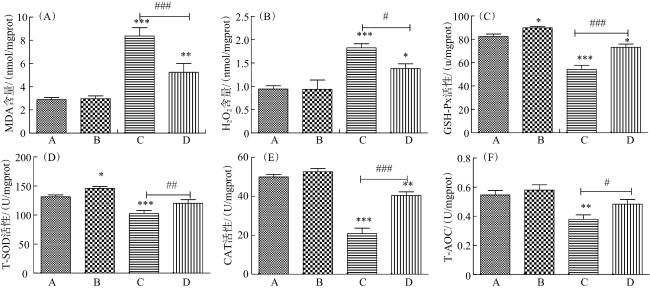
1.5 鹌鹑肝脏组织抗氧化指标测定
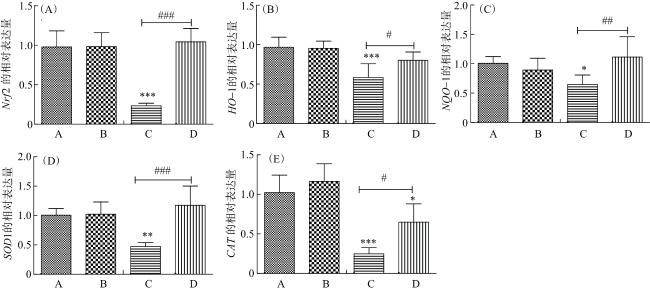
1.6 肝脏Nrf2抗氧化通路相关基因表达
表1 RT-qPCR引物信息 |
| 引物名称 | 引物序列(5'→3') |
|---|---|
| β-actin | F:CATCAGGGTGTGATGGTTGGT R:GGGGTACTTCAGGGTCAGGA |
| GAPDH | F:CTTTCCGTGTGCCAACCC R:CAGCAGCCTTCACTACCCTC |
| Nrf2 | F:TTGGCAGAAGCATTCCCGTT R:CAATCTGATCGGGAACCAGT |
| HO-1 | F:ACTTCTATGGCAGCAACTGG R:AGGTCTCCCAAATAGCGAGT |
| NQO-1 | F:CTCCGAGTGCTTTGTCTACGA R:ATGGCTGGCATCTCAAACC |
| SOD-1 | F:TGTGCATGAATTTGGAGACAAC R:TTGCAGTCACATTGCCGAG |
| CAT | F:CAAGTTCCACGTTAAGACCGAT R:TAATCAGGATCAGTAGAAGCCAGT |