1 材料与方法
1.1 试验材料
1.2 试验方法
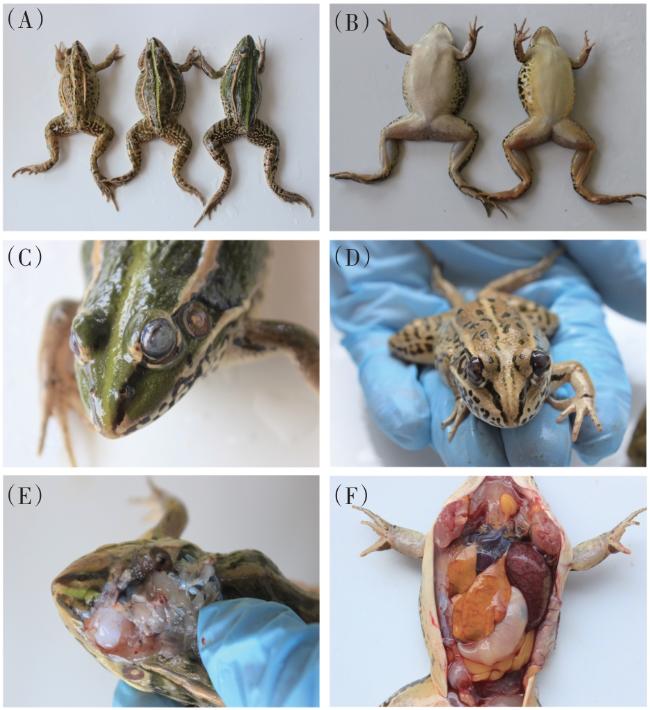
1.2.1 发病情况调查及临床病变观察
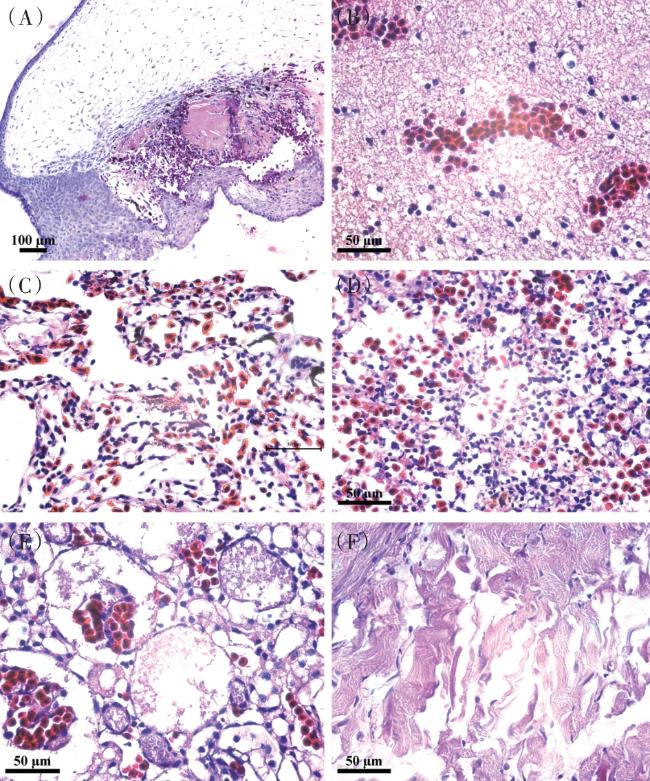
1.2.2 病理组织学观察
1.2.3 细菌分离纯化
1.2.4 细菌鉴定
表1 细菌16S rDNA和gyrB基因通用引物 |
| 引物名称 | 序列(5’—3’) | 退火温度/℃ | 预期大小/bp |
|---|---|---|---|
| 16S-F | AGAGTTTGATCCTGGCTCAG | 56 | 1 500 |
| 16S-R | TACGGCTACCTTGTTACGAC | ||
| gyrB-F | GAAGTCATCATGACCGTTCTGCAY GCNGGNGGNAARTTYGA | 56 | 1 200 |
| gyrB-R | AGCAGGGTACGGATGTGCGAGCC RTCNACRTCNGCRTCNGTCAT |
1.2.5 药敏试验
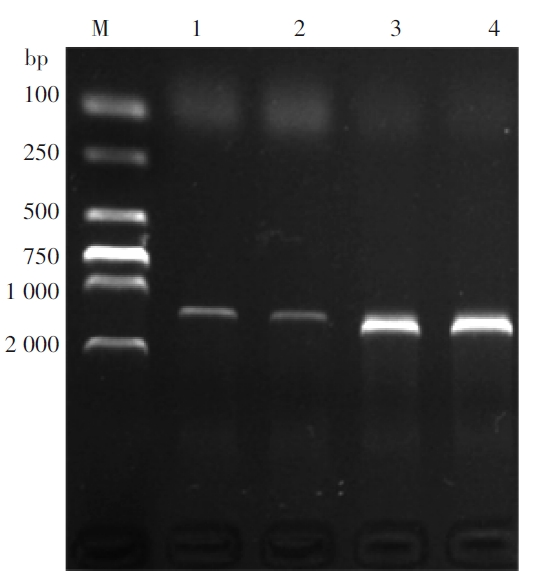
1.2.6 耐药基因检测
2 结果与分析
2.1 发病情况调查与临床病变观察
2.2 病理组织学观察
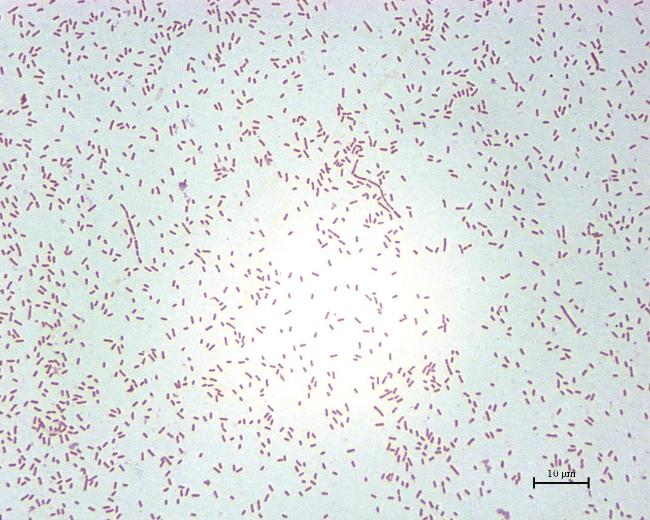
2.3 细菌分离与培养
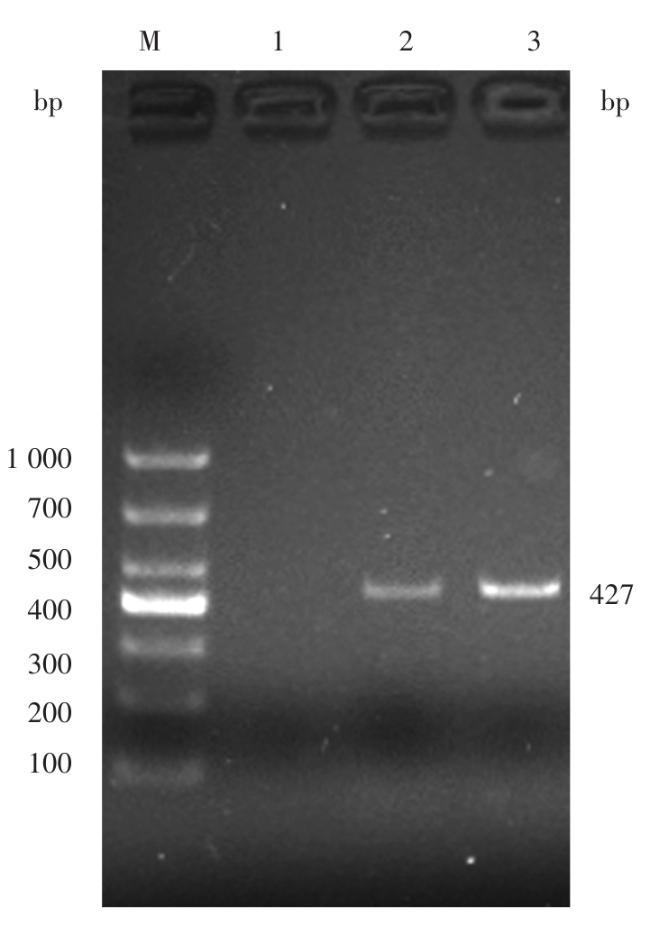
2.4 细菌鉴定
2.5 药敏试验结果
表2 病原菌药敏试验结果 |
| 抗菌药物名称 | 药敏纸片含量/(μg/片) | 抑菌圈大小/mm | 敏感 程度 |
|---|---|---|---|
| 头孢西丁(美福仙) | 30 | 26 | S |
| 阿米卡星 | 30 | 18 | S |
| 卡那霉素 | 30 | 0 | R |
| 庆大霉素 | 10 | 0 | R |
| 链霉素 | 10 | 15 | S |
| 新霉素 | 30 | 0 | R |
| 四环素 | 30 | 0 | R |
| 多西霉素 | 30 | 18 | S |
| 阿奇霉素 | 15 | 28 | S |
| 麦迪霉素 | 30 | 22 | S |
| 氟苯尼考 | 30 | 31 | S |
| 多黏菌素B | 300 IU | 0 | R |
| 两性霉素B | 30 | 0 | R |
| 诺氟沙星 | 5 | 0 | R |
| 氧氟沙星 | 5 | 0 | R |
| 洛美沙星 | 10 | 0 | R |
磺胺异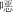 唑 唑 | 300 IU | 0 | R |
复方磺胺甲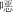 唑 唑 | 23.75/1.25 | 0 | R |
| 新生霉素 | 30 | 12 | I |
| 利福平 | 5 | 25 | S |
|
表3 病原菌抗菌肽试验结果 |
| 抗菌肽样本 | 抑菌圈直径/mm |
|---|---|
| T1 | 7 |
| T2 | 10 |
| T3 | 7 |
| T4 | 7 |
| T5 | 13 |
| 阴性对照 | 8 |