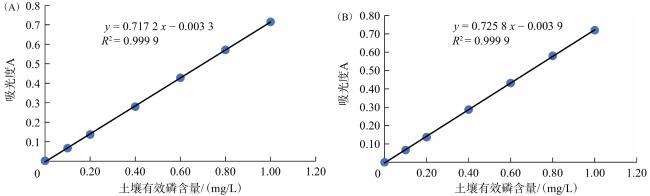
土壤有效磷测定的影响因素较多,在实际操作中要注意以下几个关键点。(1)土壤有效磷的测定值随浸提剂pH的增大而增大
[10],因此,每次浸提前要重新校正浸提剂pH,且保证同一批次的标准曲线、待测样品所使用的浸提剂一致。(2)在常规检测中,使用活性炭进行吸附可消除土壤本身的颜色干扰,但该操作过程复杂且易造成后续的污染问题。张飞龙
[11]研究表明,在880 nm波长下测定土壤有效磷时可免去添加活性炭的步骤,此波长对浸出的有机质基本无吸收。(3)浸提时需用空气浴恒温振荡器,水浴恒温振荡器批量操作时瓶子放入的深度、水浴液面保持等因素较难控制,提取温度不稳定。因此,恒温振荡器应使用校准给出的修正值。(4)碱性土壤有效磷测定的结果准确性受温度的影响较大。因此,在实验过程中对浸提温度的控制尤为重要,其中浸提温度包括房间温度、液体温度和器具温度等。白厚义等
[12]研究指出,以(25±1)℃为基准,温度每提高1 ℃土壤中的有效磷含量会增加0.43 mg/kg,这种影响会随着磷含量的不同而有所区别。实际测定时,需将室温调节至25 ℃左右,并保持使用器皿的温度与室温一致。在土壤有效磷浸提加入碳酸氢钠浸提剂前,先将恒温振荡器温度调整为(25±1)℃,将浸提剂提前放入恒温振荡器中保温。加入浸提剂前使用检定过的温度计测量液温,确保浸提剂温度控制在(25±1)℃。