1 材料与方法
1.1 试验材料
1.2 试验方法
2 结果与分析
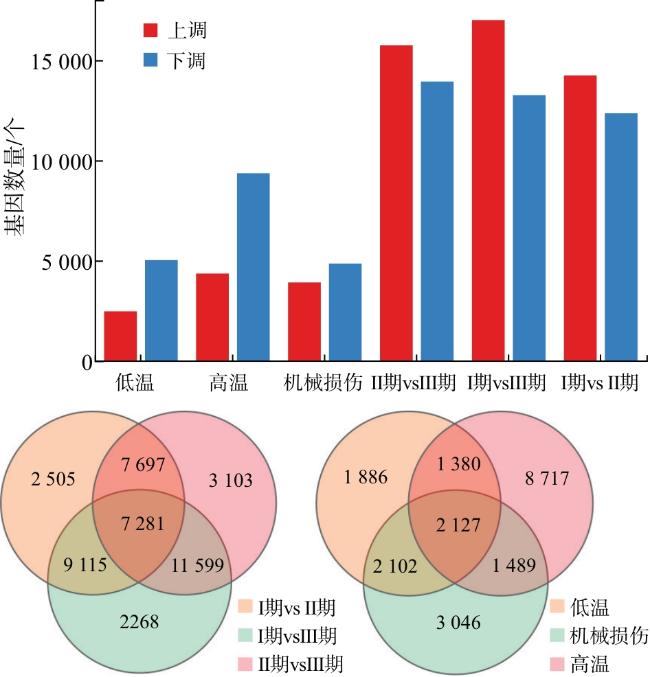
2.1 差异表达基因
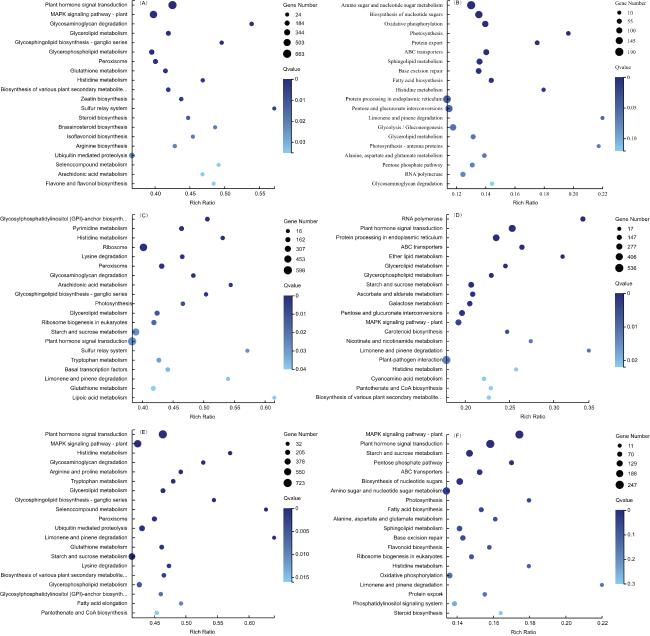
2.2 DEGs的功能聚类和调控通路
表1 差异表达基因的GO聚类单位:个 |
| 样本 | 生物过程 | 细胞组分 | 分子功能 | |||
|---|---|---|---|---|---|---|
| 细胞过程 | 代谢过程 | 细胞解剖实体 | 蛋白复合物 | 催化活性 | 结合 | |
| Ⅰ期vsⅡ期 | 5 092 | 4 734 | 7 633 | 857 | 7 055 | 6 931 |
| Ⅱ期vsⅢ期 | 5 820 | 5 290 | 8 269 | 1 085 | 7 582 | 7 621 |
| Ⅰ期vsⅢ期 | 5 675 | 5 242 | 8 572 | 953 | 7 885 | 7 743 |
| 低温 | 1 529 | 1 375 | 1 918 | 238 | 1 852 | 2 208 |
| 高温 | 2 463 | 2 202 | 3 589 | 295 | 3 293 | 3 842 |
| 机械损伤 | 1 688 | 1 520 | 2 373 | 244 | 2 198 | 2 560 |
2.3 MADS转录因子的差异表达分析
表2 MADS家族差异表达 |
| 基因编号 | 基因注释 | logFC | |||||
|---|---|---|---|---|---|---|---|
| I期vs II期 | II期vs III期 | I期vs III期 | 低温 | 高温 | 机械损伤 | ||
| DN10042_c0_g1_i1-55A | MADS2 | -4.86 | 9.76 | 4.9 | -2.99 | -9.76 | -5.95 |
| DN1068_c0_g3_i1-55A | MADS21 | 8.47 | 8.47 | -2.03 | -8.47 | -8.47 | |
| DN1068_c1_g1_i1-55A | AGL6 | 2.90 | 3.08 | 5.98 | |||
| DN1074_c1_g1_i1-55A | MADS16 | 12.26 | 12.26 | ||||
| DN1074_c1_g1_i13-55A | MADS16 | 6.81 | 6.10 | -2.23 | |||
| DN1074_c1_g1_i14-55A | MADS16 | 8.56 | 8.56 | -2.09 | |||
| DN1074_c1_g1_i4-55A | MADS16 | 10.2 | 9.58 | -2.11 | |||
| DN1074_c1_g1_i5-55A | MADS16 | -4.09 | 10.17 | 6.08 | |||
| DN11957_c0_g1_i1-57A | CAULIFLOWER A转录变体X1 | -7.08 | 4.81 | -2.27 | |||
| DN11957_c0_g1_i2-57A | CAULIFLOWER A转录变体X1 | -2.16 | |||||
| DN1256_c0_g1_i6-60A | MADS50转录变体X6 | 2.29 | |||||
| DN1256_c0_g1_i9-60A | MADS50转录变体X6 | 2.27 | 3.24 | ||||
| DN15170_c0_g1_i1-55A | MADS AGL29部分 | -2.73 | |||||
| DN1559_c0_g4_i1-59A | MADS2转录变体X1 | 4.76 | 4.05 | ||||
| DN1624_c0_g6_i1-56A | MADS16 | 2.34 | -2.29 | ||||
| DN16321_c2_g1_i1-55A | MADS JOINTLESS转录变体X1 | -4.77 | 3.78 | ||||
| DN1867_c0_g1_i1-55A | MADS box AP3-类似蛋白A | 3.15 | 3.30 | 6.45 | |||
| DN1867_c0_g1_i2-55A | MADS16类似 | 9.68 | 9.68 | ||||
| DN1867_c0_g2_i1-55A | MADS16 | 2.40 | |||||
| DN1867_c0_g2_i2-55A | MADS16 | 9.87 | 9.87 | -2.64 | |||
| DN19438_c0_g2_i1-60A | MADS SVP转录变体X2 | 12.78 | |||||
| DN22662_c0_g1_i1-59A | MADS SVP转录变体X3 | 3.45 | 2.14 | -7.69 | |||
| DN23575_c0_g1_i3-57A | MADS AGL29部分 | -3.08 | -4.75 | -7.83 | 4.75 | ||
| DN23575_c0_g1_i4-57A | MADS AGL29部分 | -7.11 | 5.98 | -5.98 | |||
| DN25403_c0_g1_i1-60A | CAULIFLOWER A转录变体X2 | 11.99 | -11.99 | ||||
| DN25676_c0_g1_i1-59A | MADS32 | 7.51 | -2.70 | 4.81 | 3.05 | ||
| DN2791_c0_g1_i3-56A | CAULIFLOWER A | -2.05 | -3.53 | -4.58 | -4.58 | -4.58 | |
| DN28168_c0_g1_i1-58A | MADS SVP转录变体X2 | 2.35 | |||||
| DN2980_c0_g3_i3-55A | MADS SOC1 | -2.34 | |||||
| DN3067_c0_g3_i1-57A | MADS JOINTLESS转录变体X1 | -9.85 | 5.04 | -4.80 | -5.04 | ||
| DN3067_c0_g3_i2-57A | MADS JOINTLESS转录变体X1 | -6.73 | -6.16 | ||||
| DN3262_c0_g2_i1-59A | MADS16 | 3.30 | -3.39 | ||||
| DN3262_c0_g2_i2-59A | MADS16 | 2.64 | 3.91 | -2.08 | -2.03 | ||
| DN353_c0_g1_i12-56A | MADS16 | 7.55 | -12.9 | -5.36 | 6.19 | 4.46 | 3.32 |
| DN353_c0_g1_i13-56A | MADS16 | 9.91 | -9.91 | 5.95 | 3.91 | 5.78 | |
| DN353_c0_g1_i3-56A | MADS16 | 10.45 | -10.45 | 3.91 | 4.58 | ||
| DN353_c0_g1_i4-56A | MADS16 | 5.98 | -5.98 | 3.46 | |||
| DN353_c0_g1_i9-56A | APETALA3-类似蛋白3_2 | 8.92 | 7.94 | -7.94 | |||
| DN37239_c0_g1_i1-56A | CAULIFLOWER A-类似转录变体X2 | 3.92 | 3.60 | ||||
| DN432_c0_g2_i2-57A | MADS16 | 2.90 | -2.32 | -2.04 | -2.58 | ||
| DN4759_c0_g1_i1-57A | CAULIFLOWER A | -3.08 | -2.16 | -5.23 | |||
| DN4759_c0_g1_i2-57A | CAULIFLOWER A | -3.40 | -4.72 | -4.32 | -4.32 | -4.32 | |
| DN4759_c0_g1_i3-57A | CAULIFLOWER A | -9.73 | -9.73 | ||||
| DN4987_c0_g1_i2-59A | MADS EJ2 | 2.26 | |||||
| DN5334_c0_g1_i2-57A | MADS3类似 | -9.98 | 3.70 | -6.28 | 2.96 | -3.70 | -3.70 |
| DN5334_c0_g1_i3-57A | AGAMOUS-类似蛋白 | -7.06 | 4.58 | -2.48 | -3.68 | -7.58 | -3.68 |
| DN5334_c0_g2_i1-57A | AGAMOUS类似 | -8.64 | -8.64 | 7.10 | 5.49 | ||
| DN5334_c0_g2_i2-57A | AGAMOUS类似 | -7.89 | 5.32 | -2.57 | -5.32 | -5.32 | |
| DN5338_c0_g1_i1-60A | MADS SOC1 | -3.63 | |||||
| DN5338_c0_g2_i3-60A | MADS SOC1 | -2.62 | -2.38 | ||||
| DN5352_c1_g3_i1-55A | MADS CMB1 | 2.32 | |||||
| DN556_c0_g1_i3-60A | MADS16 | 6.02 | 4.49 | -2.45 | |||
| DN556_c0_g1_i5-60A | MADS16 | 7.92 | 8.96 | ||||
| DN5588_c0_g1_i1-57A | MADS6 | -3.62 | -2.62 | -3.35 | |||
| DN578_c0_g1_i4-57A | MADS AGL9同源 | -7.27 | -6.62 | ||||
| DN6272_c0_g1_i2-58A | MADS EJ2 | -2.62 | 2.52 | ||||
| DN7049_c0_g2_i1-57A | MADS AGL65 | -3.81 | -5.23 | ||||
| DN8879_c0_g1_i1-59A | MADS类似 | 7.43 | |||||
| DN9010_c0_g3_i1-56A | MADS AGL9同源 | -2.91 | -2.04 | ||||
| DN9010_c0_g3_i3-56A | MADS AGL9同源 | -2.64 | |||||
| DN9157_c0_g2_i2-58A | MADS3类似 | -8.77 | 6.87 | 2.15 | -6.87 | ||