运城盐湖位于山西省运城市南郊(110°52′—111°00′ E,34°35′—35°49′ N),是硫酸钠型内陆湖
[1]。该湖泊是重要的食盐产地,目前主要生产芒硝和硫酸镁
[2]。因采用“垦畦浇晒法”产盐,盐湖被分成了大小不等的区域,每个区域的湖水盐度有所不同,且湖水盐浓度变化较大,这会对其中微生物的生态群落分布及多样性造成影响
[3]。采盐、采硝等活动在盐湖东部区域持续进行,导致其景观与生态环境同其他盐湖相比大不相同。因此,运城盐湖生态体系可能孕育独特的微生物类群,其中的微生物可以适应高盐环境,同时具有耐低温、耐高温、抗辐射和耐有机溶剂等特点,其研究和开发价值较大
[4]。
黑泥是一种湖底沉积物,是运城盐湖的独特资源。目前对运城盐湖的相关研究主要集中在污染物分析
[5]、藻类植物
[6-7]、卤虫
[8-9]等方面,但关于黑泥微生物资源暂无深入和系统地研究。Zhang等
[10]从运城盐湖黑泥中分离出一株新型中度嗜盐菌C176T,经鉴定为螺杆菌属的一个新种。Su等
[11]分离并鉴定了一株耐盐放线菌CFH 90308(T),发现其次生代谢产物对枯草芽孢杆菌、丁香假单胞菌、嗜水气单胞菌和抗药性金黄色葡萄球菌均具有抑菌活性。Cui等
[12]分别从运城盐湖沉积物和新疆塔里木盆地盐渍土中分离得到4株嗜盐古菌YCN1(T)、YCN58(T)、LT38(T)和LT62(T),并通过表型特征、系统发育属、系统基因组属和比较基因组分析,进行菌株分类鉴定。Guo等
[13]从运城盐湖沉积物中成功分离出了首个新属级物种,并将其命名为
Yunchengibacter salinarum YC-2023-2T。Zeng等
[14]利用宏基因组学技术对运城盐湖盐渍土壤中嗜盐细菌的多样性进行了分析;李坤珺等
[15]采用克隆文库技术对运城盐湖水和淤泥混合样品的嗜盐细菌菌群组成进行了研究。
运城盐湖黑泥富含对人体皮肤有益的矿物质、微量元素及有机质,可用于发用清洁护理产品
[16]、面膜
[17]中,具有清洁保湿、抗菌修护等天然功效,开发利用价值较大。天然黑泥中含有大量微生物,必须进行灭菌处理才能符合应用要求
[18]。常规的灭菌方法是高压蒸汽法,而矿泥中的一些有益有机质可能在热处理下降解,因此也有报道采用辐照法等灭菌方法
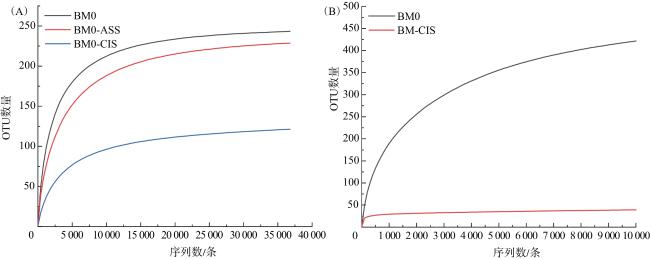
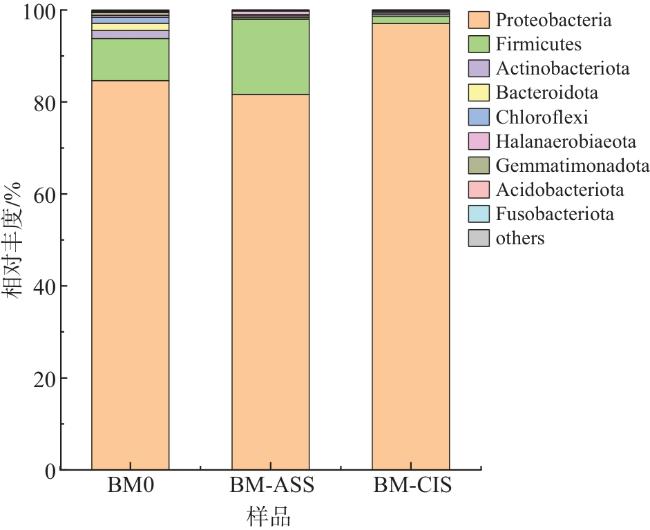
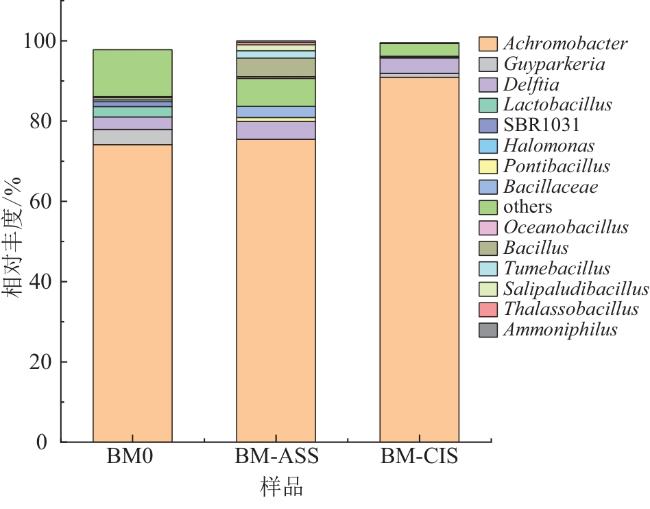
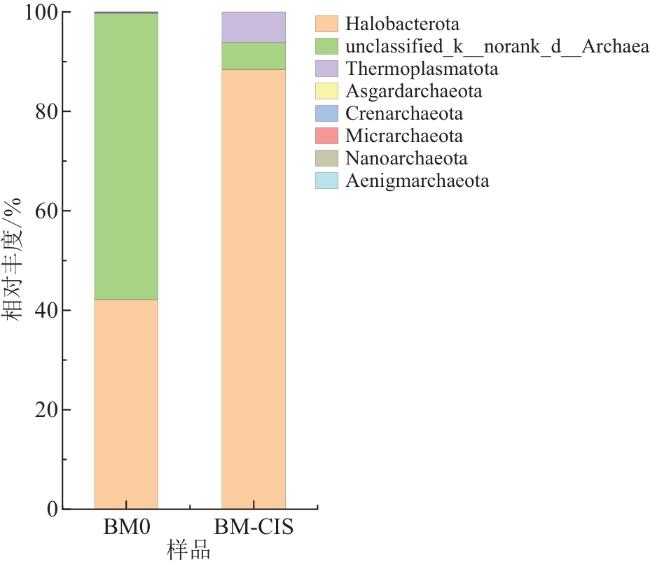
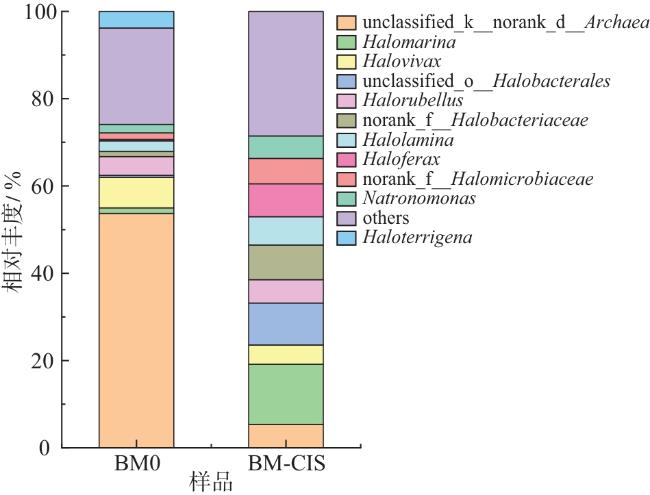
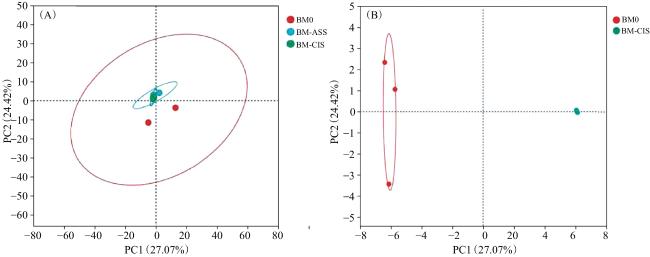
[19]。本研究利用高通量测序技术分析运城盐湖黑泥及两种不同灭菌方式处理的泥样中细菌和古菌的群落组成,并研究不同灭菌方式对细菌和古菌群落结构的影响,为运城盐湖黑泥资源的开发利用提供参考。