化学感受系统在昆虫觅食、求偶、产卵以及躲避天敌和有毒物质等生物学过程中起着关键作用
[1-3]。昆虫主要借助触角等嗅觉器官对寄主植物进行远距离定位,依靠口器、足等化学感受器官进行近距离食物评估
[4-5]。大量研究证实,部分鳞翅目昆虫降落于植物表面后,常以足碰触寄主叶片,感知其表面的信息化学物质,进而评估食物的安全性和可食用性,甚至判断该寄主植物是否适宜其幼虫取食
[6-8]。因此,昆虫的足在味觉感知、寄主植物选择和产卵偏好中发挥着重要作用。
昆虫足化学感受功能的实现主要依赖于几个功能上相互关联的基因家族,包括气味结合蛋白(Odorant binding proteins,OBPs)、化学感受蛋白(Chemosensory proteins,CSPs)、气味受体(Olfactory receptors,ORs)、味觉受体(Gustatory receptors,GRs)、离子型受体(Ionotropic receptors,IRs)和感觉神经元膜蛋白(Sensory neuron membrane proteins,SNMPs)等
[9-11]。杨叶青等
[12]研究发现,中红侧沟茧蜂(
Microplitis mediator)OBP19主要在前足跗节的感器下方表达,能与非挥发物和挥发物结合,参与味觉识别过程。Hua等
[13]研究表明,在绿盲蝽(
Apolygus lucorum)雄虫足中高表达的气味结合蛋白AlucOBP9与植物挥发物有较强的结合能力,暗示绿盲蝽足部参与了近距离识别化学信息物质的过程。果蝇足中的多种化学感受相关蛋白与求偶行为相关,如在果蝇雄虫前足特异表达的GR68 a直接参与雌虫性信息素的识别
[14]。可见,这些基因家族在化学感受过程中发挥着不同作用,深入研究昆虫化学感受相关蛋白对揭示昆虫化学感受机理具有重要作用。
小菜蛾(
Plutella xylostella)是十字花科植物专食性的农业害虫。作为鳞翅目昆虫,其雌雄成虫利用其灵敏的化学感受系统完成各自重要的生命活动
[15-16]。小菜蛾雌虫将异硫氰酸酯类物质作为嗅觉信号,用于远距离寻找寄主植物,当其降落到寄主植物所在位置后,通过触角或足触碰叶片,以芥子油苷作为味觉信号刺激自身产卵
[17-19];而小菜蛾雄虫则以雌虫释放的性信息素为信号,准确定位雌虫并与之交配,进而维持种群繁衍
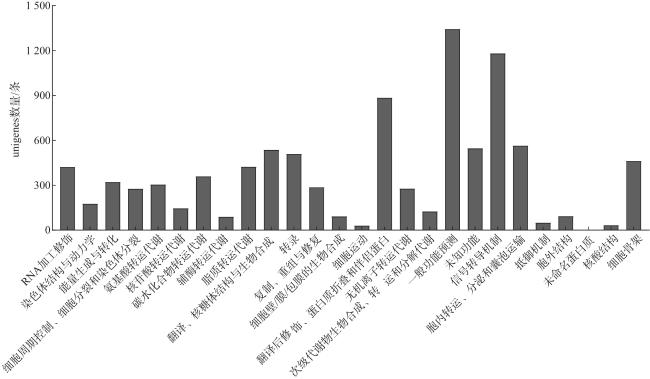
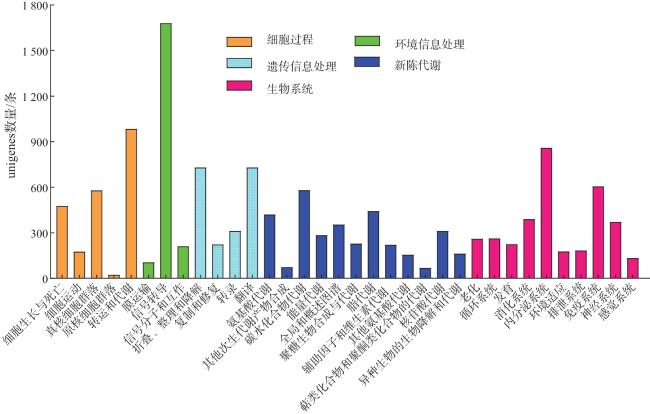
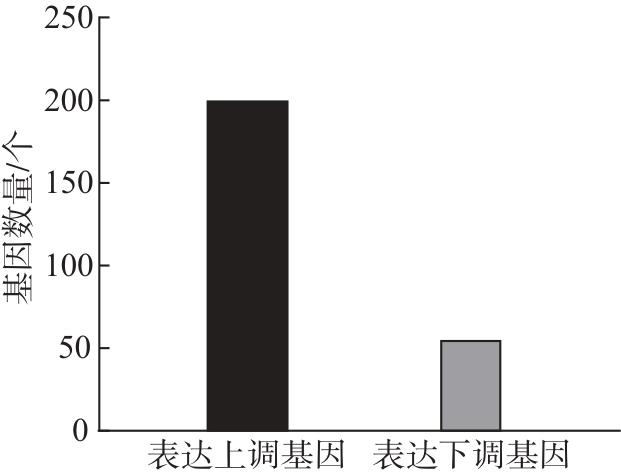
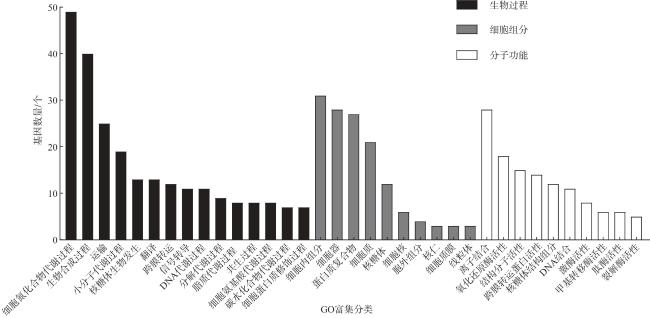
[20]。为初步解析小菜蛾雌、雄成虫足在化学感受过程中的分子机制,本研究收集了小菜蛾雌、雄成虫足样品,利用Illumina NovaSeq 6000测序系统进行转录组测序,将获得的序列进行拼接和组装,并进行基因功能注释和功能分类,深入挖掘其中的差异表达基因,获得了与小菜蛾化学感受功能相关的差异表达基因,为进一步了解小菜蛾感知外界信息化学物质的机制提供参考。