1 材料与方法
1.1 试验地基本情况
1.2 试验材料
1.3 试验设计
1.4 样品采集与处理
1.5 测定方法
1.5.1 植株茎秆微生物基因组DNA的提取及检测
1.5.2 PCR产物的混样和纯化
1.5.3 文库构建和上机测序
1.6 数据分析
2 结果与分析
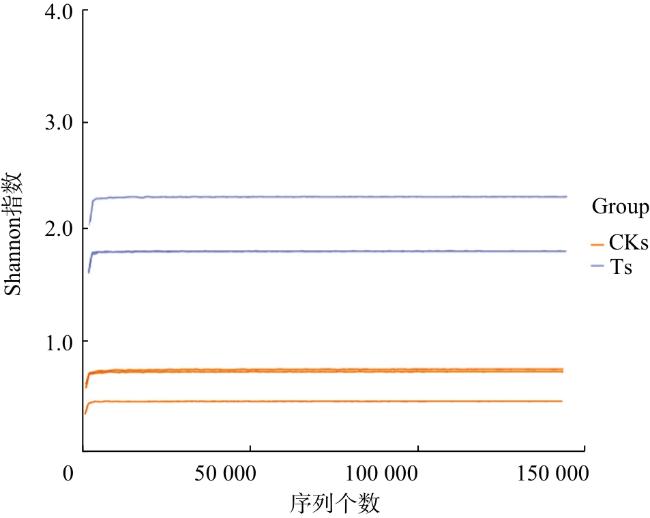
2.1 茄子茎秆内生细菌Alpha多样性分析
表1 感病与未感病茄子茎秆内生细菌Alpha多样性特征 |
| 处理 | 多样性指数 | ||||
|---|---|---|---|---|---|
| 有效序 列/条 | OTUs总数 | Chao1指数 | Shannon指数 | 测序深度 | |
| CKs1 | 194 117 | 454 | 681 | 0.75 | 0.99 |
| CKs2 | 199 888 | 179 | 262 | 0.41 | 0.99 |
| CKs3 | 210 091 | 339 | 528 | 0.70 | 0.99 |
| Ts1 | 204 724 | 188 | 269 | 1.81 | 0.99 |
| Ts2 | 209 145 | 253 | 318 | 2.33 | 0.99 |
| Ts3 | 188 979 | 390 | 519 | 1.82 | 0.99 |
|