1 材料与方法
1.1 试验鱼类及前处理
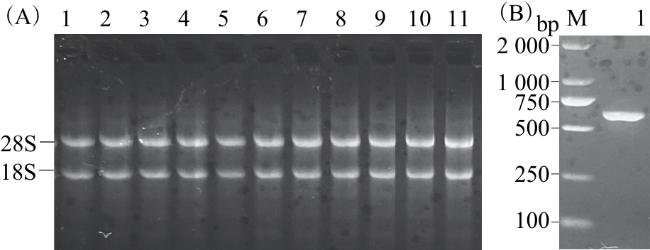
1.2 总RNA的提取与反转录
1.3 Lcak1基因CDS的克隆
1.4 Lcak1基因的序列特性分析
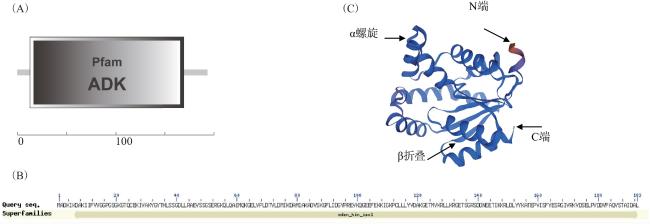
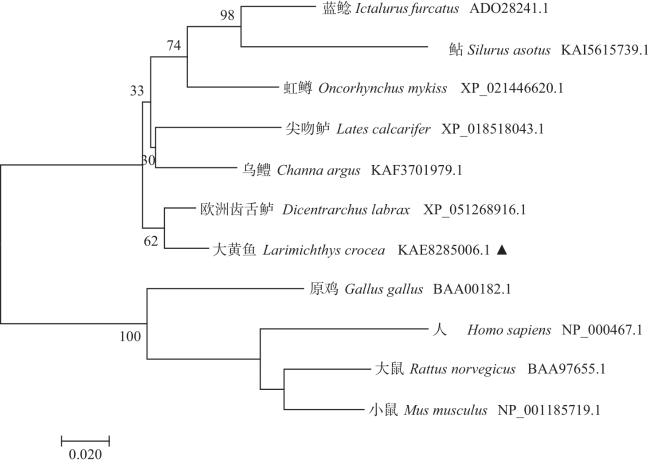
1.5 LcAK1蛋白结构与进化分析
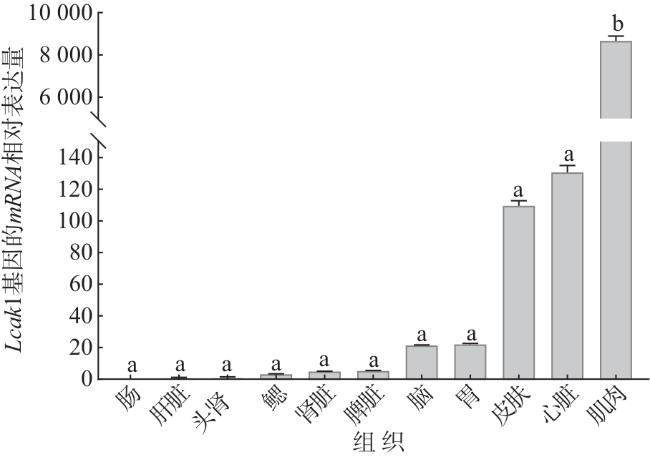
1.6 Lcak1基因表达模式分析
表1 Lcak1基因的qPCR引物 |
| 引物名称 | 引物序列(5'-3') | 基因编号 | 用途 |
|---|---|---|---|
| qLcak1-F | GAAGCGCCTGGACCTGTATT | XM_019276271.2 | 目的基因qPCR扩增 |
| qLcak1-R | CAATGCCTCGGCTCTCATAA | ||
| qLcβ-actin-F | GACCTCACAGACTACCTCATG | GU584189.1 | 内参基因qPCR扩增 |
| qLcβactin-R | TGTTGTAGGTGGTCTCGTGGA |